При неревизионной операции при раке легкого основой лечения становится комплексный подход, который включает адъювантную или неоадъювантную химиотерапию, а также лучевую терапию. Химиотерапия может быть назначена для уменьшения размеров опухоли перед операцией или для предотвращения рецидива после операции. Лучевая терапия, в свою очередь, может использоваться для контроля локализации болезни и облегчения симптомов.
Кроме того, важно учитывать индивидуальные особенности пациента, такие как общее состояние здоровья, стадия заболевания и биологические характеристики опухоли. Паллиативные методы, включая симптоматическое лечение, также могут быть включены в лечение для повышения качества жизни пациента и снижения эмоционального стресса.
- Не радикальная операция при раке легкого предполагает применение дополнительных методов лечения.
- Адъювантная химиотерапия может улучшить выживаемость пациентов после операции.
- Лучевая терапия часто используется для контроля локального прогресса опухоли.
- Иммунотерапия и таргетная терапия могут быть эффективными при определенных мутациях.
- Мультидисциплинарный подход важен для выбора оптимальной схемы лечения.
- Регулярное мониторирование состояния пациента помогает своевременно адаптировать тактику лечения.
Какие бывают стадии и их особенности:
- На I стадии в легких формируется небольшая опухоль, которая не превышает 3-4 см в диаметре. Метастазирование в лимфатические узлы и другие органы отсутствует. Обычно новообразование удается удалить полностью при помощи хирургического вмешательства.
- II стадия диагностируется, когда размер опухоли достигает 4-7 см, и метастазы начинают затрагивать прилегающие лимфатические узлы.
- На III стадии рак начинает распространяться в пространство между легкими и трахеей, затрагивая ближайшие лимфоузлы. Размер опухоли превышает 5 см.
- IV стадия устанавливается, если метастазы находят свое место в других органах.
Выбор лечения всегда определяется лечащим врачом отдельно для каждого конкретного пациента. На это решение влияет множество факторов, которые можно разделить на следующие группы:
- Характер и распространенность опухолевого процесса
- Биологические характеристики опухоли
- Особенности пациента
Характер и распространенность опухолевого процесса:
- стадия заболевания (см. выше);
- расположение опухолей в организме (например, если опухоль расположена рядом с крупным сосудом, это может повлиять на возможность хирургического вмешательства).
Биологические характеристики опухоли
- тип рака легкого (см. выше);
- наличие специфических биомаркеров в опухоли.
Особенности пациента:
- общее состояние здоровья при начале лечения;
- возраст и наличие сопутствующих заболеваний;
- другие препараты, принимаемые пациентом.
Рак легкого диагностируется по результатам комплексного обследования. Рентгеновского снимка и заключения патолога со словом “рак” для назначения лечения недостаточно.
Знание не только стадии и типа опухоли, но и её молекулярных и генетических характерistik является важным аспектом для индивидуализации лечения. Каждый пациент должен получить уникальную терапию, соответствующую его потребностям.
Опухоли легких могут различаться по наличию различных биомаркеров — специфических генов или белков, в том числе аномальных, которые возникают при мутациях. Для их выявления у пациентов с диагнозом рак легкого проводят молекулярно-генетическое тестирование.

В России молекулярно-генетическое тестирование для пациентов предоставляется бесплатно. С 2020 года врачи могут осуществлять тестирование за счет средств обязательного медицинского страхования. Также активно реализуется федеральная программа «Совершенствование молекулярно-генетической диагностики в Российской Федерации для повышения эффективности противоопухолевого лечения». В рамках данной программы онкологи в России имеют возможность направлять образцы своих пациентов на молекулярно-генетическое исследование (www.cancergenome.ru). Эта программа также доступна для пациентов без оплаты.
Врач может назначить молекулярно-генетические тесты, рекомендованные при вашем типе опухоли. Например, при неплоскоклеточном раке легкого алгоритм тестирования обычно выглядит следующим образом:
- В первую очередь следует выяснить, есть ли у опухоли мутации в гене EGFR (рецепторе эпидермального роста), так как изменения в этом гене являются наиболее распространенными для целевых препаратов.
- Если мутации не обнаружены, врач может провести анализ на транслокации, касающиеся гена ALK (рецептора тирозинкиназы анапластической лимфомы).
- При отсутствии транслокаций ALK выполняется тест на мутации в гене ROS1.
- Если мутации не найдены, то тестируют на BRAF-v600.
Иммунотерапия при раке легкого
При наличии рака легкого опухолевые клетки начинают экспрессировать PD–L1. Этот белок в здоровом организме защищает клетки от аутореактивных Т-лимфоцитов. Опухолевые клетки тренируются экспрессировать PD–L1 на поверхности, что позволяет им избегать иммунного ответа организма.
Выделяют три группы по уровням экспрессии:
- Отрицательная (<1%)
- Позитивная (≥1%) – пембролизумаб может назначаться при непереносимости химиотерапии
- Высокая позитивная (>50%) говорит о том, что пембролизумаб может быть назначен как препарат первой линии. Ожидается более выраженный ответ на лечение.
Препарат Ниволумаб может применяться только начиная со второй линии терапии, независимо от уровня экспрессии PD–L1.
При разработке тактики лечения при не радикальной операции при раке легкого, необходимо учитывать множество факторов, таких как стадия заболевания, общее состояние пациента, сопутствующие патологии и тип опухоли. Я считаю, что основным приоритетом должно быть комплексное подход к лечению, который включает не только химиотерапию, но и лучевую терапию. Эти методы могут помочь в контроле прогрессии заболевания и обеспечении качественной жизни пациента.
Важно отметить, что не радикальная операция, например, лобэктомия или сегментарная резекция, может быть выполнена у пациентов, у которых рак легкого находится на ранних стадиях и имеются противопоказания для радикального вмешательства. В таких случаях сочетание хирургического лечения с последующей адъювантной химиотерапией или лучевой терапией позволяет снизить риск рецидива. Я также уделяю особое внимание монитированию ответной реакции на лечение, так как это может потребовать корректировки в тактике ведения пациента.
Кроме того, следует учитывать и индивидуальные характеристики каждого пациента. Например, при наличии метастазов или первичного рака, невзирая на проведённую операцию, необходимо активно включать таргетную и иммунотерапию. Перспективным направлением является использование биомаркеров для более точного выбора схемы лечения. Такой подход позволяет оптимизировать результаты и повышает шансы на длительную ремиссию даже в ситуациях, когда полное удаление опухоли невозможно.
Осложнения иммунотерапии
Иммунотерапия делает опухолевые клетки видимыми для иммунной системы, что приводит к разрушению опухолевых клеток Т-лимфоцитами. Однако активизация иммунной системы может вызвать и «гипереактивность», при которой здоровые клетки организма станут восприниматься как чуждые. Поэтому побочные эффекты иммунотерапии могут включать аутоиммунные реакции.
Признаки возникновения осложнений появляются чаще после 2-3 циклов лечения, на 2-3 неделе после последнего введения препарата. Пострадать может любой орган, но чаще всего симптомы проявляются в отношении кожи или желудочно-кишечного тракта. Это могут быть реакции со стороны кожи — сыпь, угри, зуд. При нетяжелом варианте не требуют отмены лечения, с симптоматической целью принимаются антигистаминные препараты.
Серьезные иммуноопосредованные осложнения со стороны ЖКТ могут быть угрожающими жизни. Сюда относятся тошнота и рвота, а также частый или жидкий стул с кровью или слизью. Важно оперативно уведомить врача о таких симптомах. При запущенных случаях могут возникнуть язвы или трещины в стенках кишечника.
При поражении печени проявляются тяжесть в правом подреберье, желтуха и небольшая тошнота. Биохимический анализ крови в таких случаях покажет повышение уровней АлТ, АсТ и общего билирубина. Поэтому мониторинг лабораторных показателей перед каждой терапией имеет огромное значение.
Осложнения со стороны почек и эндокринной системы встречаются реже. Их симптомы могут напоминать обычные недомогания: головные боли, утомляемость, снижение аппетита и слабость, что может привести к их игнорированию. Эти проблемы часто обнаруживаются лишь при контроле лабораторных исследований или обследовании функции щитовидной железы.
Гормональный профиль исследуется до начала лечения иммунопрепаратами и 1 раз в 1,5-3 месяца после начала терапии.
Серьезные осложнения также могут возникнуть со стороны дыхательной системы. Пневмонит — это неинфекционное воспаление легких, проявляющееся одышкой и периодическим сухим кашлем. Врач в таком случае обязан провести дополнительные исследования, назначить рентген или компьютерную томографию легких.
Поскольку причина всех этих осложнений заключается в чрезмерной активации иммунной системы, лечение будет состоять в подавлении иммунного ответа с помощью глюкокортикоидов, которые применяются только под контролем лечащего врача-онколога. Иммуноопосредованные осложнения могут возникнуть как в первые недели и месяцы терапии, так и спустя 2-3 года после ее завершения.
Рак легких. Симптомы, лечение, диагностика, операция

Диагноз «рак легких» пугает, устрашает и обескураживает, но в этой статье мы попытаемся объяснить, почему этот действительно серьезный диагноз не должен заставить пациента опустить руки и сдаться, расскажем, как можно добиться хороших результатов лечения и в каких случаях после радикального лечения можно на многие годы забыть об этом заболевании.
Главным условием успешного лечения рака легкого является как можно более раннее обращение за медицинской помощью к специалистам. В отдельном разделе данной статьи мы детально обсудим методы терапии рака легкого, но уже сейчас отметим, что хирургия остается наиболее эффективным методом лечения.
В нашей стране остается актуальной проблема, что время от появления опухоли до обращения пациента к торакальному хирургу может быть заметно затянутым. К сожалению, это часто приводит к тому, что на момент обращения к хирургу опухоль оказывается уже запущенной, и хирургическое вмешательство становится невозможным В этом виновата и сама опухоль: рак легкого может длительное время протекать без явных симптомов, и быстро давать метастазы.
Но и наши пациенты в силу особенностей российского менталитета не обращают внимание на грозные симптомы, терпят до последнего, не хотят расстраивать близких и избегают обращения к врачам. С другой стороны после выявления опухоли (при флюорографии, рентгенографии, компьютерной томографии, бронхоскопии) обескураженному, потерянному пациенту и его родственникам предстоит пройти бесчисленное количество «комиссий» и «консультаций».
Некоторые пациенты, столкнувшись с долгим процессом обращения в клиники, могут стать отчаявшимися и прекратить лечение, в то время как случаются и ситуации, когда через 2-3 месяца пациенту все же удается попасть на лечение. Однако 2-3 месяца для рака легкого — это недопустимый срок. За это время опухоль может существенно увеличиться, дать метастазы и стать недоступной для хирургического удаления.
В нашем Центре созданы оптимальные условия для того, чтобы максимально сократить временной промежуток между постановкой диагноза и началом лечения. Если диагностика выявляет у пациента с раком легкого возможность проведения радикальной операции, такие пациенты могут быть госпитализированы в наш Центр в приоритетном порядке: с момента первой консультации до поступления в стационар проходит не более недели. В hospital ситуации, в течение 10-12 дней осуществляется всестороннее обследование, по окончании которого принимается решение о наиболее подходящей терапии для конкретного клиента.
Какие же шаги предстоит пройти пациенту с серьезным диагнозом «рак легкого» для получения наилучшего результата? Все процедуры и методы лечения можно условно выделить на три основные группы: подтверждение диагноза «рак легкого», стадирование опухоли и выбор необходимой терапии.
• Подтверждение диагноза «рак».
Диагноз «рак легкого» в основном устанавливается на основе результатов рентгенографии, компьютерной томографии (КТ) и ПЭТ. Специалисты по лучевой диагностике часто употребляют такие термины, как «новообразование», «Neo» и «Са» в качестве синонимов данного диагноза (см. рис. 1, рис. 2, рис. 3).

Рис. 1. ПЭТ-КТ всего тела — это современный высокоточный метод, используемый для диагностики рака легкого и оценки его распространенности.

Рис. 2. КТ-картина периферической опухоли левого легкого. В ходе обследования у пациента выявлены множественные метастазы в лимфоузлах средостения, больному было проведено химио-лучевое лечение.

Рис. 3. Позитронная эмиссионная томография 72-летнего пациента О. с большой периферической опухолью в верхней доле правого легкого. Анализы показали, что это плоскоклеточный рак. В ходе видеомедиастиноскопии метастазы в лимфоузлах средостения не обнаружены. В апреле 2007 года пациент успешно перенес операцию в нашем Центре, в ходе которой была проведена расширенная верхняя лобэктомия справа.

При контрольном осмотре в 2013 году состояние пациента было удовлетворительным; рецидив опухоли отсутствует.
Однако, несмотря на высокую точность современных методов обследования, диагноз «рак легкого» остается предварительным и неокончательным (хоть и высоковероятным), до тех пора пока не выполнена надежная биопсия опухоли, то есть не получен кусочек новообразования для подробного исследования под микроскопом. Только после обнаружения в этом «кусочке» опухолевых клеток диагноз становится окончательным.
В нашем Центре применяются современные методы малоинвазивной биопсии, которые помогают поставить диагноз как при опухолях крупных бронхов (центральный рак), так и в периферических участках легкого. Фибробронхоскопия, включая чрезбронхиальную биопсию, занимает центральное место в диагностике опухолей легких (см. рис. 4, рис. 5).
Иногда требуется использовать различные способы чрезкожной игловой биопсии. В некоторых случаях ни один из современных диагностических методов не позволяет подобраться к сложно расположенной опухоли. В таких случаях, после полного обследования (в котором учитываются КТ, ПЭТ и фибробронхоскопия), биопсия может быть выполнена во время лечебно-диагностической операции.

Рис. 4. Фибробронхоскопия у 59-летнего пациента М. с центральным раком левого легкого. Опухоль растет в трахею и не может быть хирургически удалена. Для поддержания дыхательных путей в нашем Центре пациенту был установлен самораскрывающийся стент в трахею, после чего его направили на химиолучевое лечение.

Рис. 5. У пациента К., 65 лет при компьютерной томографии выявлено периферическое образование в верхней доле левого легкого (А, Б). Для окончательной установки диагноза выполнена бронхоскопия с чрезбронхиальной биопсией (В), при которой подтверждена аденокарцинома (злокачественная опухоль) легкого. В марте 2013 года пациент успешно прооперирован в нашем Центре — выполнена расширенная видеоторакоскопическая верхняя лобэктомия слева.

• Оценка стадии опухоли.
Ключевым компонентом предоперационного обследования пациентов с злокачественными опухолями является стадирование заболевания, то есть оценка степени распространенности рака (прорастание в соседние органы, наличие метастазов в лимфатических узлах и удаленных органах). Стадия опухоли напрямую определяет прогноз и выбор оптимальной схемы лечения.
При раке легкого вопросы стадирования особенно остры и актуальны, так как цена решения о выполнении/невыполнении операции очень высока, а значит, от того насколько правильно и точно проведено стадирование зависит адекватность и эффективность лечения. Для предоперационного стадирования пациентов с раком легкого в нашем Центре разработан алгоритм, который согласуется с европейскими рекомендациями.
У ряда пациентов комбинация данных КТ и ПЭТ бывает достаточно для определения стадии рака, однако в большинстве случаев для точной оценки стадии необходимо проводить незначительную диагностическую операцию — видеомедиастиноскопию (см. рис. 6). Эта процедура позволяет выполнить биопсию лимфатических узлов средостения. Мы накопили и проанализировали обширный опыт применения видеомедиастиноскопии при раке легкого в нашем городе. Результаты нашего исследования подтвердили, что выполнение такой операции перед крупной хирургической интервенцией на легком способствует улучшению отдаленных результатов лечения.

Рис. 6. Видеомедиастиноскопия – диагностическое вмешательство, результаты которого определяют тактику лечения и целесообразность хирургического вмешательства. А – введение медиастиноскопа в средостение через маленький разрез на шее. Б – биопсия лимфоузлов под видео контролем.
В – эндоскопическая картина во время операции: 1 – левый главный бронх, 2 – правый главный бронх, 3 – бифуркационные лимфоузлы, 4 – легочная артерия. Г – операция завершается наложением косметичного внутрикожного шва, практически незаметного на коже.
В лечении рака легкого применяются хирургия, лучевая и химиотерапия. Хирургическое вмешательство является наиболее эффективным методом терапии на I-II стадиях опухоли, когда хирурги удаляют пораженные части легкого (долю) или целиком легкое, а также лимфатические узлы средостения. При ранних стадиях рака легкого пятилетняя выживаемость после операции достигает 75-80%. Для снижения травматичности операций в нашем Центре активно используются видеоторакоскопические методы, которые значительно уменьшают операционную травму, болевой синдром после операции и снижают риск осложнений, сокращая тем самым восстановительный период.
При принятии решения о проведении операции важно учитывать не только распространенность опухоли, но и возможность организма пациента выдержать запланируемое вмешательство, что в торакальной хирургии называется «функциональной операбельностью». Мы уделяем серьезное внимание оценке функциональной операбельности, применяя различные методы для определения функциональных резервов организма.
Результаты обследования каждого пациента обсуждаются на клиническом разборе и онкологической комиссии, где после тщательного обсуждения принимается окончательное решение. Если хирургическое лечение представляется оптимальным, операция выполняется без задержек нашими торакальными хирургами (см. рис. 7). В случаях, когда после операции или вместо нее требуется химиолучевая терапия, пациента направляют в ведущие онкологические центры нашего города.

Рис. 7. Малоинвазивная радикальная операция при раке легкого – видеоторакоскопическая нижняя лобэктомия слева, выделение легочной артерии.
Методы лечения на различных стадиях болезни
1 и 2 стадии
При лечении рака легкого на 1-2 стадии обычно используются такие методы как хирургическое вмешательство и лучевая терапия.
Объем хирургического вмешательства зависит от стадии и локализации новообразования:
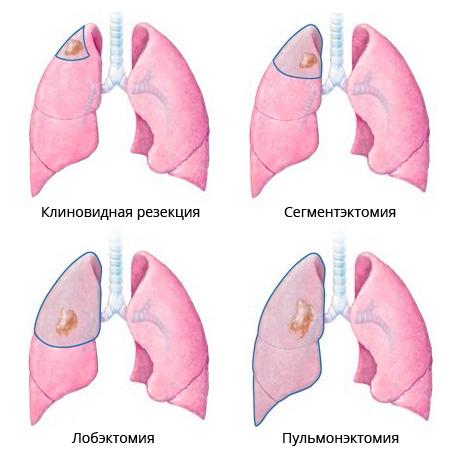
- Частичное удаление. При наличии возможности врачам удается удалить только небольшую часть (клиновидная резекция), затронутый сегмент (сегментэктомия), долю (лобэктомия) или даже две доли (билобэктомия). Одна из ключевых задач после подобных операций состоит в том, чтобы помочь пациенту «раздышать», то есть вернуть дыхательным органам их полную функциональность. Полное удаление. В некоторых случаях может потребоваться удалить весь орган (пульмонэктомия), часто вместе с ближайшими лимфатическими узлами. Такая операция обычно показана при диагностике бронхогенной карциномы.
- Декомпенсированные формы сердечной и дыхательной недостаточности;

Недостатками данного подхода являются его травматичность и высокий риск послеоперационных осложнений, однако его преимуществом является возможность радикального решения проблемы.
В ряде случаев стандартную операцию проводить оказывается невозможно. Наиболее частые противопоказания к хирургическому вмешательству:
- близость к сердцу, аорте и другим крупным сосудам, нервным сплетениям;
- непереносимость наркотических средств и другие.
В таких случаях прибегают к стереотаксической радиохирургии: высокоточному облучению очага большими дозами радиации (лучевая терапия Киберножом). При необходимости этот метод сочетается с назначением курса моделируемой по интенсивности лучевой терапии (ЛТ).
К основным достоинствам новых технологий относятся:
- небольшое повреждение здоровых тканей;
- возможность повышения дозы облучения до терапевтически эффективного уровня.
Для закрепления результатов радиохирургии и лучевой терапии может использоваться химиотерапия (по показаниям).
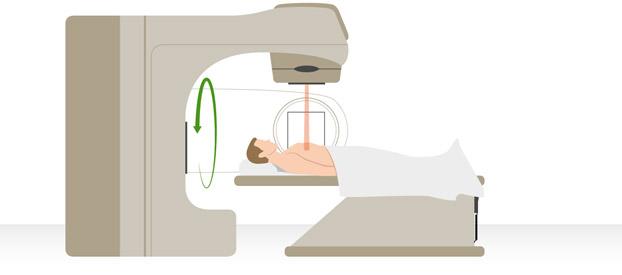
При мелкоклеточном раке легкого обычно назначаются курсы лучевой терапии и химиопрепараты (тиофосфамид, 5-фторурацил).
Наиболее оптимально лечение плоскоклеточного рака легкого на ранних стадиях (0-1): прогноз в целом благоприятный для всех случаев, большинство больных достигают устойчивой ремиссии. При выявлении рака на 2 стадии дать однозначный прогноз сложно: это зависит от типа заболевания.
Методы, применяемые на 3-4 стадии
- Комплексное лечение при раке легких на 3 стадии с метастазами в региональные лимфоузлы включает комбинацию лучевой и химиотерапии. Кроме того, пациенту, исходя из показаний, могут назначаться симптоматические процедуры (лечебные пункции плевральной полости для удаления накопившейся жидкости, назначение средств для остановки кровотечений и др.).
- Методы лечения рака легкого на 4 стадии с метастазами в отдаленные органы аналогичны предыдущим, включая устранение сопутствующих симптомов. Тактика лечения формируется в зависимости от текущих проблем и состояния пациента.
- Схема и состав терапии при обнаружении метастазов в легких из других органов определяются после выяснения их происхождения и степени поражения.
Вероятность достижения ремиссии у больных с метастатическими опухолями значительно ниже, чем у пациентов на 1-2 стадиях, прогноз по лечению местно-распространенной плоскоклеточной формы заболевания умеренно оптимистичный. Тем не менее, грамотно организованная помощь даже на 4 стадии с метастазами и поражением соседних органов может замедлить прогрессирование болезни у 10% пациентов (в зависимости от типа новообразования). Таким образом, у больного с любой стадией и формой заболевания есть шанс на жизнь.
Последствия терапии и восстановление
Вероятность и характер осложнений после лечения рака легких зависят от поставленного диагноза, состояния пациента, а также методов и объема терапии.
Среди преходящих побочных эффектов чаще всего наблюдается повышенная утомляемость и одышка. К нарушениям, требующим коррекции, относятся послеоперационный ателектаз, развитие абсцессов или плеврита в отдаленном периоде после ЛТ и др.
Скорость и качество восстановления зависят от соблюдения назначений врачей. В частности, необходимо полностью отказаться от курения, увеличить уровень физической активности в разумных пределах, скорректировать режим питания и состав рациона. Важно придерживаться расписания профилактических медицинских осмотров.
Если вам необходимо получить второе мнение для уточнения диагноза или плана лечения, отправьте нам заявку и необходимые документы для консультации, либо запишитесь на личную встречу по телефону.
Опыт других людей
Алексей, 45 лет: «Когда мне поставили диагноз рак легкого, я был в шоке. Врач предложил не радикальную операцию, так как опухоль была в труднодоступном месте. Мы начали с химиотерапии, чтобы уменьшить размер опухоли. После нескольких курсов реакция была положительной, и я прошел курс лучевой терапии. Я активно следил за своим состоянием и консультировался с врачами относительно дальнейших шагов. В итоге опухоль уменьшилась, и мне сделали операцию для удаления остатков. Я стараюсь следить за своим здоровьем и поддерживать психологическую устойчивость.»
Мария, 38 лет: «Когда я узнала о необходимости не радикальной операции, я была безумно напугана. Однако врачи объяснили, что в моем случае это будет лучший вариант, чтобы не подвергать организм чрезмерным нагрузкам. Начали с предоперационного курса химиотерапии, который помог снизить размеры опухоли. Затем мне делали таргетную терапию, и опыт ее применения показал свою эффективность. Поддержка семьи и друзей была очень важна для меня – это помогло справиться с психологическими трудностями. Я очень благодарна своему врачу, который сумел найти правильный подход к лечению.»
Сергей, 50 лет: «Раковую опухоль обнаружили случайно, когда я проходил плановое обследование. После биопсии выяснилось, что операция может быть не совсем радикальной. Мне предложили комбинированный подход: сначала химиотерапия, затем при необходимости лучевая терапия. Я скептически относился к химиотерапии, но врач объяснил, что это поможет увеличить шансы на успех операции. После курсов химио я заметил улучшения, и потом мне провели операцию с минимальным вмешательством. Применяли метод лапароскопии. Я не ожидал, что лечение будет таким эффективным и безболезненным.»
Вопросы по теме
Как влияет выбор тактики лечения на качество жизни пациентов после не радикальной операции при раке легкого?
Выбор тактики лечения, в первую очередь, влияет на качество жизни пациентов через управление симптомами и побочными эффектами. Если после не радикальной операции применяются методы adjuvant терапии, такие как химиотерапия или лучевая терапия, это может значительно уменьшить вероятность рецидива заболевания, но также может вызывать побочные реакции. Важно учитывать баланс между эффективностью лечения и возможными осложнениями, чтобы пациенты могли сохранить активное участие в жизни и поддерживать приемлемый уровень комфорта. Дополнительные психосоциальные меры, такие как поддержка психолога или групповой терапии, также могут способствовать улучшению качества жизни.
Какие альтернативные методы могут рассматриваться при не радикальной операции при раке легкого?
При не радикальной операции важно рассмотреть альтернативные методы лечения, такие как таргетная терапия, иммунотерапия и клинические испытания новых препаратов. Например, таргетные препараты могут быть эффективны для пациентов с определенными генетическими мутациями. Иммунотерапия, в свою очередь, может активировать собственные защитные силы организма для борьбы с раковыми клетками. Клинические испытания могут предложить доступ к новейшим медикаментам и стратегиям, что становится важной опцией для пациентов, у которых традиционные методы лечения не привели к желаемым результатам.
Как часто следует проводить контрольные обследования после не радикальной операции для оценки эффективности лечения?
Контрольные обследования после не радикальной операции должны проводиться регулярно, обычно с интервалом 3-6 месяцев в первый год. После этого, в зависимости от состояния пациента и ответа на терапию, обследования могут реорганизовываться на годовые периоды. Важной частью наблюдения являются как рентгенографические исследования, так и круги лабораторных анализов для оценки функционирования органов и выявления потенциальных рецидивов. Раннее обнаружение возможных осложнений и рецидивов существенно повышает шансы на успешное восстановление и дальнейшее лечение.




