Состояние пациента после лечения опухоли мочевого пузыря с установкой нефростомы может варьироваться в зависимости от стадии заболевания и общего состояния здоровья. Нефростома позволяет выполнять отток мочи, что способствует предотвращению инфекций и снижению нагрузки на мочевыводящие пути. Однако данный процесс требует регулярного наблюдения и ухода, чтобы избежать осложнений.
Постоперационный период может сопровождаться дискомфортом и необходимостью адаптации к новым условиям жизни. Важно следить за функционированием нефростомы и соблюдать рекомендации врача, что поможет успешно вернуться к привычной жизни и минимизировать возможные осложнения.
- Нефростомия применяется как временная мера при лечении опухолей мочевого пузыря.
- После процедуры важно следить за состоянием пациента и возможными осложнениями.
- Профилактика инфекций и контроль состояния почек являются ключевыми аспектами послеоперационного ухода.
- Регулярное наблюдение и диагностика необходимы для оценки рецидива опухоли.
- Реабилитация включает психологическую поддержку и адаптацию к измененному образу жизни.
Диагностика и лечение урологических осложнений рака предстательной железы
Рак предстательной железы (РПЖ) по-прежнему является важной темой в области уроонкологии и урогериатрии. Увеличение продолжительности жизни и старение населения, характерные для развитых стран, способствуют возрастанию случаев онкологии, в том числе и РПЖ.
Каждый год в пяти ведущих европейских странах фиксируют 80 тысяч новых случаев РПЖ и 45 тысяч летальных исходов, связанных с данным заболеванием [50]. В России, по данным 1992 года, RПЖ составлял 2,9% в общей структуре онкозаболеваний, в то время как к 1995 году этот показатель возрос до 3,8%. В онкоурологической практике в 1992 и 1995 годах соответственно показатели составили 36% и 41%. За последние десять лет частота обнаружения РПЖ удвоилась [3]. В период с 1989 по 1996 год число впервые зарегистрированных случаев выросло с 5,5 тыс. до 8,3 тыс., что соответствует 52% увеличению.
Средний возраст пациентов с РПЖ в России составляет 69 лет, а для тех, кто умер от этой болезни, — 70 лет; в США эти показатели равны 72 и 77 годам соответственно. Из-за особенностей клинического течения, опухоль нередко долгое время не проявляется, и симптомы могут наблюдаться только у 8-10% пациентов. При этом риск смерти от РПЖ снижается до 30%.
За последние годы, благодаря внедрению в клиническую практику новых методов диагностики (ТРУЗИ, КТ, МРТ, исследование концентрации ПСА крови), значительно чаще стали выявлять заболевание на более ранних стадиях.
Тем не менее, 50-70% пациентов обращаются за лечением именно из-за осложнений, связанных с РПЖ.
На сегодняшний день не разработана четкая клиническая классификация осложнений РПЖ, что может помешать формированию универсального подхода к диагностике и, что самое главное, к оказанию специализированной медицинской помощи, принимая во внимание временной фактор диагностики.
Нарушения мочеиспускания — самый распространенный симптом (60-80%) при РПЖ. Причиной его является раковая обструкция. Под обструктивными формами РПЖ подразумевают такие формы роста опухоли, которые нарушают свободный отток мочи по мочевым путям:
— инфравезикальные (обструкция в области пузырно-уретрального сегмента);
— суправезикальные (сдавление мочеточников опухолью);
— комбинация этих двух типов обструкции.
При этом частота инфравезикальной обструкции, по сообщениям различных авторов, варьирует от 17 до 72%, суправезикальной обструкции — от 2 до 51%.
Патогенез таких состояний на фоне РПЖ имеет многоаспектный характер и включает в себя не только механическое воздействие – сдавление и изменение угла между уретрой и мочевым пузырем, но и нарушения кровообращения в области тазовых вен на фоне хронического воспаления предстательной железы.
Процесс опорожнения мочевого пузыря также подвергается своеобразным изменениям. Для обеспечения мочеиспускания детрузорный компонент процесса может усиливаться с развитием гипертрофии, а затем прогрессивно и неадекватно снижаться, создавая условия для суб- и декомпенсации с появлением и увеличением количества остаточной мочи [4, 7].
Инфравезикальная обструкция в пузырно-уретральной зоне может быть вызвана как механическими факторами — доброкачественной гиперплазией или РПЖ, так и динамическими, связанными с повышенным тонусом гладкой мускулатуры шейки мочевого пузыря и простаты [1, 7, 50]. Наблюдения показывают, что ухудшение ситуации при РПЖ происходит быстрее, чем при других состояниях, вызывающих инфравезикальную обструкцию [7].
Общепризнанно, что лечение больных с инфравезикальной обструкцией должно начинаться как можно раньше, еще до возникновения осложнений болезни. Поэтому, весьма важным является раннее ее выявление. Это необходимо и для установления этиологического диагноза, и для определения тактики лечения больных [2].
Постепенное или резкое снижение функциональных резервов детрузора может привести к острой задержке мочи [7]. Согласно данным Маринбаха Е. В., это состояние наблюдается примерно у 20% пациентов с РПЖ [34]. Симонов В. Я. и Козлов В. А. зафиксировали острое нарушение мочеиспускания у 12% таких больных [33].
По наблюдениям Аляева Ю. Г. и соавт. острая задержка мочеиспускания, которая может быть первым симптомом рака предстательной железы или возникнуть на фоне его лечения, возникает в 15-20% случаев [3]. Катетеризация мочевого пузыря, в этих ситуациях, может привести к восстановлению мочеиспускания или переходу в фазу хронической задержки мочи [7, 31]. При этом, на фоне снижения сократительной способности детрузора постепенно нарастает количество остаточной мочи и нарушение функции верхних мочевых путей.
Многочисленные исследования показывают, что обструкция нижних мочевых путей, помимо дизурии, провоцирует нарушения уродинамики в верхних мочевых путях (мочеточниках и почках) [54]. Зубко В. И. указывает на высокую степень этих нарушений (53,2%), среди которых наиболее распространены односторонний или двусторонний уретерогидронефроз [22].
Гидронефроз и уретерогидронефроз обычно развиваются бессимптомно. Однако, при анализе секционных карт умерших от РПЖ пациентов гидронефроз встречался в 9,7% случаев [45]. Клинических признаков, характерных только для этих состояний, нет [25, 30, 42].
Для точной оценки состояния верхних мочевых путей следует использовать диагностику, которая подтвердит диагноз и выяснит причины возникновения состояния, а также стадию его развития. Первоначально нужно провести ультразвуковое исследование [30]. Оно позволяет определить размеры почечных лоханок и чашечек, а также степень их расширения и толщину паренхимы. Комбинация УЗИ с экскреторной урографией и радиоизотопной нефросцинтиграфией формируют первую группу стандартного обследования, которое способно дать качественные данные о функциональных расстройствах [11, 39].
С помощью комбинации различных методов можно дать ответ на основные диагностические вопросы, связанные с характеристикой уродинамических расстройств, а именно: определить характер нарушения (обструктивный или динамический), выявить локализацию и гидродинамическую значимость имеющегося препятствия, а также охарактеризовать выраженность функциональной недостаточности и определить функциональные резервы верхних мочевых путей.
Это особенно важно, поскольку уростаз и увеличение дилатации верхних мочевых путей приводят к снижению кровоснабжения коры почки и венозной стазе в медуллярной зоне [7]. Подобные механизмы при хронической задержке мочи могут спровоцировать воспалительные процессы, такие как пиелонефрит [22, 24].
Многие авторы указывают на возможность развития хронического пиелонефрита при бесконтрольном применении или использовании ударных доз эстрогенов, вызывающих дистрофические изменения в почках [21,43] и снижение тонуса мочеточников [5]. Лейзеруков Е. М. наблюдал признаки пиелонефрита у 71% больных, получающих эстрогенотерапию по поводу РПЖ, в то же время у 50% из них отмечалось расширение верхних мочевых путей [28].
Согласно данным Самсонова В. А., среди осложнений РПЖ пиелонефрит наблюдается в 51,7% случаев [45]. Автор отмечает, что этот инфекционный процесс в большинстве случаев обусловлен колибациллярной инфекцией. Особенностями хронического пиелонефрита у пациентов с инфравезикальной обструкцией и нарушениями уродинамики верхних мочевых путей являются устойчивое течение, частые рецидивы и стойкость к антибиотикотерапии [53]. Активный инфекционный процесс в мочеполовых органах во время хирургического вмешательства способствует развитию кровотечений, септических реакций (которые составляют 4,8% всех летальных исходов от РПЖ [45]), тромбоэмболий (2,8% случаев смерти от РПЖ [45]), а также недержанию мочи [14].
Хронический пиелонефрит является одной из основных причин инвалидизации урологических больных вследствие развития в основном хронической почечной недостаточности, доля которой составляет 21-25% [15], вплоть до уремии [30]. При анализе секционных карт в исследованиях Самсонова В. А. отмечено, что уремия явилась результатом пиелонефрита и гидронефроза в каждом четвертом случае РПЖ [45].
Следует отметить, что некоторые пациенты, поступающие с урологическими осложнениями, могут уже иметь установленный диагноз РПЖ и, возможно, проходить какое-либо лечение. В таком случае важно наличие алгоритма диагностики для проверки данных пациентов. Однако большинство из них (50-70%) — это пациенты без подтвержденного диагноза РПЖ. В этом случае необходимо провести этиологическую диагностику для определения правильной тактики комплексного лечения, основываясь на анамнезе и результатах обследования, что может указывать на наличие РПЖ как одну из причин описанных жалоб.
При возникновении подозрения на РПЖ в первую очередь принято проводить три необходимых обследования:
1. Пальцевое ректальное обследование. По данным Матвеева Б. П., его специфичность составляет 37,9% [36], а по данным Хурсевича Н. А. и его коллег — 10,7% [46].
2. Определение уровня концентрации ПСА крови имеет наименьшее количество ложно-отрицательных результатов и наибольшую специфичность. Увеличение уровня ПСА до больших значений (около 20 нг/мл и выше) является высокоспецифичным даже при нормальных показателях ректального исследования [18, 27].
3. Трансректальное ультразвуковое исследование предстательной железы. Специфичность данного метода при диагностике РПЖ составляет 20-30% [36]. В исследованиях, проведенных Громовым А., показатели эффективности ультразвукового метода диагностики РПЖ были следующими: чувствительность — 70,2%, специфичность — 98,4%, точность — 98,1%, прогностическая ценность положительного результата — 43,4% [17]. Хурсевич Н. А. и его коллеги определили информативность ультразвукового метода на уровне 27,7% [46]. Использование допплеровских методик в сочетании с трансректальным исследованием предоставляет дополнительную информацию для выявления опухоли предстательной железы [29, 48].
Особое место в диагностике РПЖ занимает морфологическое подтверждение диагноза, основанное на исследовании материала полученного при биопсии. Благодаря оптимальному сочетанию низкой травматичности и информативности наиболее распространённой методикой является пункционная биопсия предстательной железы.
Этиология
В настоящее время причины возникновения рака мочевого пузыря изучены не до конца. Среди доказанных факторов риска развития рака мочевого пузыря можно выделить:
- курение (в 20-65% случаев),
- профессиональные риски в 20-25% случаев (работа в отраслях с использованием химикатов и текстиля),
- лучевая терапия при других онкологических заболеваниях (рак гинекологических органов — в 2-4 раза чаще, рак предстательной железы и другие),
- хронические инфекции мочевыводящих путей,
- шистосомоз (увеличивает риск рака мочевого пузыря почти в 5 раз),
- химиотерапия при онкологии других органов,
- опухоли верхних мочевых путей (почки, мочеточники),
- мужской пол,
- хроническая задержка мочи в мочевом пузыре.
Состояние после лечения опухоли мочевого пузыря с использованием нефростомии может варьироваться в зависимости от стадии заболевания, общего состояния пациента и выбранной тактики лечения. Как правило, нефростомия выполняется для обеспечения оттока мочи в случаях, когда нормальное функционирование мочевыводящей системы нарушено. Эта процедура может привести к значительному улучшению качества жизни, снижая риск осложнений, таких как инфекции мочевых путей и гидронефроз.
После операции пациент часто сталкивается с рядом новых ощущений и проблем, связанных с наличием нефростомической трубки. Важно отметить, что уход за нефростомой требует тщательности и аккуратности. Я рекомендую тщательно следить за состоянием кожных покровов в области выхода трубки и обеспечивать надлежащее удаление мочи, чтобы избежать заражения. Также необходим регулярный осмотр у врача, который сможет оценить состояние пациента и при необходимости скорректировать лечение.
Кроме того, эмоциональное состояние пациента после лечения опухоли мочевого пузыря также требует внимания. Часто пациенты испытывают тревогу и стресс по поводу изменений в своем здоровье и необходимости постоянного медицинского контроля. Я всегда подчеркиваю важность поддерживающей терапии и общения с квалифицированными специалистами, которые смогут предложить психологическую помощь и рекомендации по адаптации к новым условиям жизни.
Классификация
Наиболее часто используется TNM-классификация злокачественных опухолей (от англ. Tumour, Nodes, Metastases – первичная опухоль, лимфатические узлы, отдаленные метастазы).
- Т — первичная опухоль
- Тх — первичная опухоль не подлежит оценке
- Т0 — отсутствие признаков первичной опухоли
- Та — неинвазивная папиллярная карцинома
- Тis — карцинома in situ (плоская опухоль)
- Т1 — опухоль прорастает в субэпителиальную соединительную ткань
- Т2 — опухоль прорастает в мышечный слой:
- Т2а — поверхностный (внутренняя половина)
- Т2b — глубокий (наружная половина)
- Т3а — микроскопически
- Т3b — макроскопически (экстравезикальная опухолевая ткань)
- Т4а — прорастает в предстательную железу, матку или влагалище
- Т4b — прорастает в стенку таза или брюшную стенку
- N – лимфатические узлы
- Nх — регионарные лимфатические узлы не могут быть оценены
- N0 — метастазы в регионарных лимфатических узлах отсутствуют
- N1 — метастазы в одном (подвздошном, запирательном, наружном подвздошном или пресакральном) лимфатическом узле в малом тазе
- N2 — метастазы в нескольких (подвздошных, запирательных, наружных подвздошных или пресакральных) лимфатических узлах в малом тазе
- N3 — метастазы в одном общем подвздошном лимфатическом узле или более.
- М – отдаленные метастазы
- М0 — отсутствуют отдаленные метастазы
- М1 — отдаленные метастазы имеются.
I этап реабилитации
Первый этап реабилитации проходит в условиях онкоурологического отделения и начинается уже в первые часы после операции. Врачи уверены, что чем раньше человек поднимается с постели, начинает себя обслуживать и самостоятельно питаться, тем лучше. Современные клинические рекомендации предлагают начинать садиться в кровати уже через два часа после операции. Такой подход уменьшает риск венозных тромбозов и осложнений со стороны дыхательной системы, а также предупреждает потерю мышечной массы 3 .
Реабилитационные мероприятия первой стадии направлены на предотвращение застойных явлений в легких, развитие спаек в малом тазу и брюшной полости, формирование эластичного и подвижного рубца, а также улучшение работы пищеварительной системы и кровообращения [4].
Физические упражнения (ЛФК)
Физическим упражнениям отведено центральное место в реабилитации после цистэктомии. Врачи обычно рекомендуют начинать лечебную физкультуру на ранних этапах, уже в первые сутки после операции, постепенно увеличивая нагрузку 4 . Комплекс подбирают индивидуально, занятия ЛФК контролирует врач-реабилитолог. Ниже мы приведем примеры физических упражнений, которые человек может выполнять после удаления мочевого пузыря 4 .
С четвертого по седьмой день после хирургического вмешательства комплекс упражнений значительно расширяется: увеличивается как количество, так и скорость повторений для занятий, которые были предусмотрены на первые три дня (в среднем 6-8 раз с умеренной нагрузкой), некоторые из упражнений заменяются на более сложные варианты. Вариантов подходящих упражнений имеется множество, и каждый может выбрать те, которые ему более всего подходят 4 .
Физиотерапевтические методы
Со вторых-третьих суток после операции показано проведение массажа (20-минутный сеанс) и рефлексотерапии. Доказано, что их раннее применение позволяет уменьшить выраженность болевого синдрома 3,4 .
Питание
Сбалансированное питание после цистэктомии является ключом к быстрому восстановлению. Врачи стремятся как можно скорее вернуть пациента к обычному питанию per os, то есть через рот 3 .
Рацион после операции должен содержать достаточное количество энергии (25–30 ккал/кг в сутки), белка (не менее 1 г/кг, оптимально 1,5 г/кг в сутки) — основного строительного материала, витаминов и микроэлементов. При недостаточном питании врачи прибегают к дополнительному питанию, или (на медицинском языке) «нутритивной поддержке». Обычно для этих целей используют сипинги 5 .
Подробную информацию о питании после цистэктомии и нутритивной поддержке вы можете найти в специальной статье по данной теме здесь.
Психологическая поддержка
Ряд пациентов после операции переживает по поводу появившейся уростомы. На I этапе реабилитации может быть начата работа с онкопсихологом, если таковой имеется в штате больницы. Большую помощь человеку может оказать просто разговор со своими близкими. Больному после операции крайне важно понимать, что он не один, что он не становится обузой для окружающих, и жизнь продолжается.
II этап реабилитации
На втором этапе реабилитации, который охватывает примерно с 8-го по 21-й день после операции, пациент переходит в отделение реабилитации после выписки из онкоурологического отделения. Основной задачей этого этапа является улучшение качества жизни и психоэмоционального состояния пациента, а также повышение его физической выносливости и снижение риска сердечно-сосудистых осложнений 3,4 .
Физические упражнения
На этом этапе врачи рекомендуют к физическим упражнениям добавить аэробную нагрузку. Самый подходящий и доступный вариант — это ходьба. Ходить нужно хотя бы 150 минут в неделю (20–30 минут в день) 3,4 . Начинать надо с малого, постепенно увеличивая продолжительность ходьбы.
Рекомендуется заниматься физическими упражнениями 3–5 раз в неделю. Важно, чтобы выбранные упражнения вызывали интерес, поскольку это повышает шансы на продолжение занятий 4 . Можно использовать предложенный ранее комплекс.
При недержании мочи к ходьбе и физическим упражнениям нужно добавить упражнения для укрепления мышц тазового дна (Кегеля) 4 . Они помогают проводить профилактику недержания мочи и являются неотъемлемым компонентом его лечения. Лучше их сочетать с терапией с биологической обратной связью (БОС-терапией).
Упражнения для укрепления мышц области малого таза
Физиотерапевтические методы
К массажу может быть добавлена акупунктура (иглоукалывание), которая в послеоперационном периоде снижает выраженность болевого синдрома. В первые две недели по два-три сеанса продолжительностью 20–30 мин. с последующими переходом на один сеанс в неделю в течение 6–10 недель 3,4 . О возможности и необходимости проведения надо обязательно проконсультироваться с лечащим врачом.
Питание
В течение первого месяца пациент постепенно возвращается к привычному режиму питания. Диета должна быть энергетически насыщенной (25–30 ккал на килограмм массы тела в сутки), содержать достаточное количество белка (не менее 1 г на килограмм массы тела, оптимально 1,5 г на килограмм в сутки), а Витамины и микроэлементы. Если отсутствует необходимое питание, врачи могут использовать нутритивную поддержку (чаще всего с помощью сиппингов) 5 .
Более подробно о питании после цистэктомии и нутритивной поддержке читайте в тематической статье здесь.
Психологическая поддержка
У многих пациентов первые недели после операции характеризуются депрессивным состоянием, упадком сил и постоянными переживаниями о своём будущем. Это естественно, так как пациент сталкивается с изменением жизненных условий. У некоторых появляется уростома, у других — недержание мочи. Также часть пациентов испытывает страх рецидива болезни.
Чтобы человек вернулся к нормальной жизни, эти страхи и тревоги нужно нивелировать. Многим хватает бесед с родными и друзьями, ведь очень важно дать человеку выговориться, озвучить свои страхи и проблемы. Часто человек сам перебарывает этот страх и находит решение проблемы.
Если пациент не может адаптироваться к новым условиям жизни, целесообразно обратиться к онкопсихологу. В этом вопросе также могут оказать помощь пациентские организации.
Диагностика опухоли мочевого пузыря
Чтобы поставить диагноз рака мочевого пузыря, необходимо сдать мочу на цитологию, пройти экскреторной урографии, цистоскопию, эндовезикальную биопсию, УЗИ и КТ.
Цистоскопия — это эндоскопическая процедура, позволяющая визуально осмотреть внутреннюю поверхность мочевого пузыря с помощью цистоскопа. Этот метод помогает выявить опухолевую ткань и определить её локализацию, а также оценить состояние стенок пузыря и выполнить УЗИ. Кроме определения опухоли, метод может обнаружить метастазы в лимфатических узлах области таза и печени.
Рентгенологическим исследованием мочевого пузыря является компьютерная томография. Она показывает местонахождение, размеры новообразования, глубину прорастания стенки, а также метастазы в региональные лимфоузлы и в отдаленные органы. Альтернативой КТ выступает магнитно-резонансная томография.
Рентгенографическое исследование грудной клетки выполняется для выявления метастазов в легких.
Рентгенологический метод урография позволяет исследовать верхние мочевые пути – лоханки и мочеточники. Это помогает планировать будущее лечение.
Перед началом лечения рака необходимо подтвердить злокачественный характер новообразования. Для этого осуществляют цитологическое исследование мочи или биопсию опухолевой ткани с последующим гистологическим анализом.
После окончания диагностического обследования врач-уролог определяет стадию процесса. Стадирование влияет на выбор терапевтической тактики.
Лечение опухоли мочевого пузыря
Тактика лечения рака мочевого пузыря зависит от его типа: можно столкнуться с мышечно-неинвазивным или мышечно-инвазивным раком.
Если рак захватывает только слизистую оболочку, а в мышечный слой не прорастает, то это мышечно-неинвазивный рак. Он требует лечения путем выполнения трансуретральной резекции мочевого пузыря.
Если рак проникает в мышечную оболочку пузыря, это называется мышечно-инвазивным раком. Такие новообразования имеют более агрессивное течение и могут давать метастазы в лимфатические узлы таза и другие органы — печень, кости и легкие. Наилучшим методом терапии будет робот-ассистированная либо лапароскопическая цистопростатэктомия.
Трансуретральная резекция стенки мочевого пузыря
«Золотой стандарт» терапии рака мочевого пузыря — это трансуретральная резекция, другими словами, удаление участка мочевого пузыря, содержащего опухоль, эндоскопически, через уретру.
Трансуретральная резекция (ТУР) осуществляется под местным обезболиванием. Специальный инструмент (резектоскоп) вводится через уретру в пузырь, с его помощью удаляют опухоль. Сразу после резекции в пузырь вводят химиотерапевтический препарат и устанавливают катетер на срок до 5 дней.
Однако стандартное вмешательство несет немаленький риск, что опухоль рецидивирует. Ведь во время операции возникают свободно «плавающие» в содержимом мочевого пузыря злокачественные клетки. Они способны имплантироваться в слизистую оболочку вновь. Кроме этого, в результате обычной ТУР получают очень фрагментированную опухолевую ткань — ее гистологический анализ часто дает искаженные результаты. Поэтому затруднительно правильно определить стадию процесса.
Однако стандартная трансуретральная резекция не может считаться радикальным методом (полного удаления) при раке мочевого пузыря.
Лазерная en-block резекция стенки мочевого пузыря с опухолью
Преодолеть все эти минусы помогает новый метод из разряда высоких технологий — резекция стенки пузыря с опухолью единым блоком. Это означает, что опухоль убирают, не нарушая ее структуру, вместе с подстилающим слоем мышц, единым блоком. Это важно, так как не допускает образования «блуждающих» опухолевых клеток и дает показательный образец для гистологического исследования. А именно его результат становится основой стадирования болезни и назначения адекватного медикаментозного лечения.
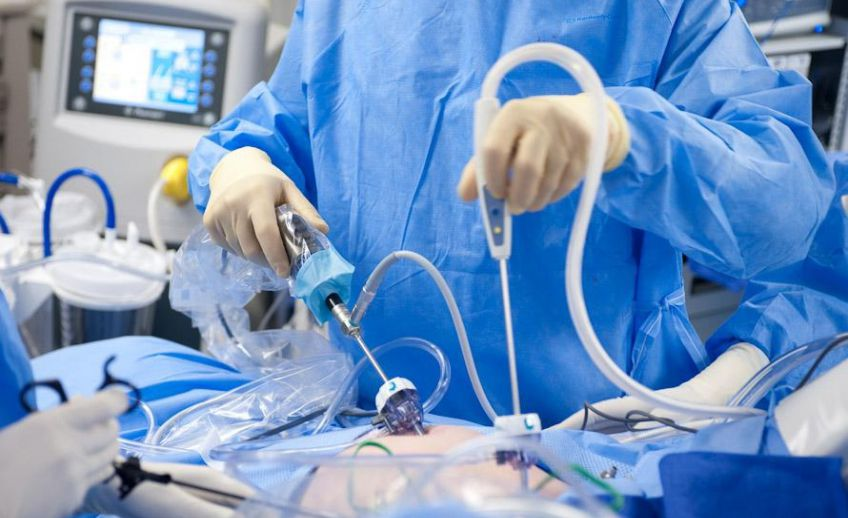
Лапароскопическая цистпростатэктомия
В этом хирургическом вмешательстве осуществляется удаление мочевого пузыря и лимфатических узлов области таза через лапароскопический доступ. У мужчин одновременно убираются простата и семенные пузырьки, а у женщин — матка с яичниками и трубами, а также передняя стенка влагалища.
После удаления мочевого пузыря необходимо наладить механизм отведения мочи — сформировать неоцистис (новый «мочевой пузырь»). Это сложнейший этап оперативного лечения.
Существуют четыре метода выполнения данной операции:
- Влажная стома: используется кусочек кишечника, из которого формируется «пузырь», который соединяется с мочеточниками и выводится на переднюю брюшную стенку; следует постоянно носить мочеприемник.
- Сухая стома: происходит то же самое, но стенки наружного отверстия формируются так, чтобы моча не вытекала сама; каждые 5 часов пациент должен вводить катетер через это отверстие для вывода мочи.
- Резервуар из прямой кишки: мочеточники пришиваются к прямой кишке, что приводит к одновременному выведению мочи и кала.
- Ортотопический «пузырь»: формируется так же, как в первых двух способах, с присоединением резервуара к уретре, что позволяет сохранять способность к самостоятельному мочеиспусканию.
Обычно после радикальной цистэктомии не требуется никакого дополнительного лечения. Однако в случае, если гистологический анализ удаленной ткани определит раковые клетки, оставшиеся по краям операционного разреза, в В околопузырной жировой клетчатке или лимфоузлах, необходимо приступить к химиотерапии.
Робот-ассистированная цистпростатэктомия
Робот-ассистированная операция является альтернативой лапароскопической цистэктомии. Она выполняется по аналогичному принципу, однако использование роботов значительно упрощает выполнение операции. Плюсами являются увеличение операционного поля в десять раз, трехмерное изображение и семиосвобожденные возможности инструментов роботов.
Рекомендации по инвазивному и метастатическому раку мочевого пузыря. Стратегии сохранения мочевого пузыря при локализованной опухоли
Почти половине пациентов с первоначальным диагнозом ИРМП стадии рТ0 или рТ1, подтвержденной при повторной резекции, после проведения только ТУР опухоли мочевого пузыря в дальнейшем требуется выполнение радикальной цистэктомии по поводу развития рецидива, при этом уровень смертности, связанной с заболеванием, в данной группе достигает 47 % [1, 2].
При диагностической ТУР критически важным моментом в принятии решения об отказе от радикальной цистэктомии является наличие или отсутствие рецидива [3, 4]. Недавние результаты 15-летнего наблюдения, проведенного Solsona [3], включали 133 пациента после радикальной ТУР мочевого пузыря с отрицательными результатами биопсии [5]. Больным проводилась регулярная цистоскопия с биопсией, и в зависимости от результата назначалось дополнительное лечение. Лишь в 6,7% случаев при первичной ТУР была недооценена стадия, у 30% больных наблюдался рецидив неинвазивного рака мочевого пузыря, что требовало внутрипузырной терапии, а у 30% произошло прогрессирование (n=40), 27 из них скончались от болезни. Пятилетняя, десятилетняя и 15-летняя канцер-специфическая выживаемость составила 81,9%, 79,5% и 76,7%, соответственно, а выживаемость без прогрессирования при сохраненном мочевом пузыре — 85,5%, 64,9% и 57,8%.
Таким образом, применение только ТУР в качестве терапевтического подхода возможно при наличии опухолей, рост которых ограничен поверхностным мышечным слоем, а В том случае, если при осуществлении диагностических биопсий не обнаруживается остаточная опухоль [6]. ТУР следует использовать в качестве единственного лечебного метода только у больных, отказывающихся от выполнения открытой операции или имеющих противопоказания к цистэктомии и комбинированной терапии для сохранения мочевого пузыря [7].
10.2. Дистанционная лучевая терапия
Поля облучения обычно включают только мочевой пузырь с запасом 1,5–2 см, при этом предполагается обязательное движение органов [1–4]. Ни разу не было продемонстрировано повышения эффективности ЛТ при увеличении полей облучения. СОД ЛТ при РМП составляет 60–66 Гр, после чего проводят дополнительное облучение мочевого пузыря или внутриполостную БТ. Ежедневная доза обычно составляет 1,8–2 Гр, при этом курс ЛТ не следует растягивать более чем на 6–7 нед — таким образом минимизируется возможность возникновения репопуляции опухолевых клеток. Использование современных стандартов и методов ЛТ приводит к развитию тяжелых поздних осложнений менее чем у 5 % больных, у которых отсутствуют признаки наличия опухоли [5–9]. Помимо эффективности применения ЛТ, к важным прогностическим факторам результатов лечения относят следующие:
- размер опухоли;
- наличие гидронефроза;
- завершенность предыдущей ТУР мочевого пузыря.
Пятилетняя общая выживаемость у больных инвазивным раком мочевого пузыря составляет от 30% до 60% в зависимости от того, был ли достигнут полный ответ на проводимую лучевую терапию, в то время как выживаемость, связанная с болезнью, составляет от 20% до 50% [10–14].
Прогностические факторы успешного лечения изучались в исследовании, проведенном одной итальянской клиникой и включавшем 459 пациентов, получавших ЛТ (примерно 30 % из них были в тяжелом состоянии с РМП стадии Т1), со средним периодом наблюдения 4,4 года. С помощью многовариантного анализа выживаемости установлены следующие статистически значимые факторы:
- возраст;
- категория T (для всех показателей эффективности лечения);
- доза облучения опухоли (только для показателей безрецидивной выживаемости) [15].
На основе имеющихся данных был проведен анализ Кокрейна, который продемонстрировал, что радикальная цистэктомия приводит к повышению общей выживаемости по сравнению с использованием только лучевой терапии [16].
ДЛТ может служить альтернативным методом лечения для пациентов с противопоказаниями к выполнению радикальной операции. Это было показано на примере группы, состоявшей из 92 пожилых или ослабленных пациентов (медиана возраста — 79 лет) с РМП стадии Т2N0–1М0. СОД — 55 Гр за 4 нед. Частота достижения полной ремиссии по данным цистоскопии через 3 мес составила 78 %, 3-летняя выживаемость без местного рецидива — 56 %, а 3-летняя общая выживаемость — 36 %. У 81 % пациентов емкость мочевого пузыря была сопоставима с показателями до начала лечения [17].
Сравнительные длинносрочные результаты также были получены автором Chung и его соавторами [18]. Всего 340 пациентов с инвазивным раком мочевого пузыря были подвергнуты только дистанционной лучевой терапии, дистанционной лучевой терапии с одновременной химиотерапией или неоадъювантной химиотерапии с последующей дистанционной лучевой терапией. Общая частота полного ответа составила 55%, а 10-летняя выживаемость по болезни и общая выживаемость составили 35% и 19% соответственно.
Полный ответ в группе только ДЛТ наблюдался в 64% случаев, в группе ДЛТ с одновременной ХТ — в 79% (n=36), а в группе неоадъювантной ХТ — в 52% (n=57), хотя в последней группе у большинства больных были стадии T3 и T4. Молодой возраст, более низкая стадия опухоли и отсутствие карциномы in situ статистически значимо коррелировали с улучшением выживаемости. Так, в группе с РМП стадии T2 5-летняя общая выживаемость составила 44%, а болезнь-специфическая — 58%. Плохим прогностическим фактором было развитие рецидива в течение 2–3 лет. Авторы пришли к выводу, что проведение ДЛТ в виде монотерапии обосновано только у тщательно отобранных пациентов.
10.2.1. Выводы и рекомендации по дистанционной лучевой терапии (табл. 10.2, 10.3)
10.3. Химиотерапия
Химиотерапия, как правило, не приводит к длительным полным ремиссиям. Некоторые исследования показывают, что частота полного ответа при химиотерапии достигает 56%, однако стоит относится к этому с осторожностью, так как вероятность ошибок при стадии существенно превышает 60% [1, 2]. Ответ на химиотерапию считается прогностическим фактором результатов лечения и продолжительности жизни [3], хотя его точность может снижается, если не учтены все показания и противопоказания.
В нескольких проспективных исследованиях были представлены результаты ХТ при операбельных (неоадъювантный метод) и неоперабельных первичных опухолях [4–7]. В ходе проведения ряда проспективных исследований после применения 2–3 циклов неоадъювантной ХТ MVAC (метотрексат, винбластин, адриамицин) или CMV (цисплатин, метотрексат, винбластин) наблюдалось снижение стадии первичной опухоли [4–6].
В исследованиях II и III фаз было установлено, что полный морфологический ответ на первичное заболевание мочевого пузыря возникает в 12-15% случаев после химиотерапии методом MVAC и в 12-22% — после GC (гемцитабин, цисплатин) [4–6, 8–16]. В последних исследованиях при проведении неоадъювантного курса химиотерапии GC, в сочетании с радикальной цистэктомией, отмечается меньший процент отрицательных результатов гистологического исследования, что может быть связано с недостаточной плотностью дозы и нежелательной отсрочкой операции [17]. Эффективность терапии с сохранением мочевого пузыря можно оценивать только с помощью цистоскопии, КТ и тщательного наблюдения. Подобный подход вызывает неточности в определении стадии, что ведет к риску местного рецидива или дальнейшего метастазирования.
В тщательно отобранных случаях стратегия сохранения мочевого пузыря, включающая ТУР и системную цисплатинсодержащую ХТ (желательно с MVAC), позволяет получить длительную выживаемость с сохраненным мочевым пузырем [18]. Тем не менее этот метод нельзя рекомендовать для применения в клинической практике.
10.3.1. Выводы и рекомендации по химиотерапии инвазивного рака мочевого пузыря (табл. 10.4, 10.5)
10.4. Мультимодальная стратегия сохранения мочевого пузыря
Комплексный метод лечения инвазивного рака мочевого пузыря (ИРМП) включает в себя трансуретральную резекцию (ТУР) первичной опухоли, химиотерапию (ХТ) и лучевую терапию (ЛТ) [1, 2]. Основной причиной использования ТУР и ЛТ является достижение локального контроля рака, тогда как главная задача системной ХТ, чаще всего реализуемой с помощью метотрексада, цисплатина и винбластина (MCV), заключается в устранении микрометастазов. В ряде методов лечения применяются цисплатин и/или 5-фторурацил, а в последнее время также гемцитабин в комбинации с ЛТ, так как они служат радиосенсибилизирующими средствами. Полная ответная реакция на лечение после проведения ТУР, последующего курса ХТ с использованием цисплатина и ЛТ, достигает 60-80%.
В небольшом исследовании I/II фазы особо подчеркивалась роль гемцитабина в комбинированной терапии, с 5-летней общей выживаемостью 70,1%, и болезнь-специфической выживаемостью 78,9% [3].
В одном из исследований с периодом наблюдения около 42 месяцев анализировались результаты комбинации ТУР с химиолучевой терапией (n=331) против ТУР с ЛТ (n=142) [4]. В общей сложности частота полного ответа оказалась высокой, составляя 70,4%, но в группе, получившей химиолучевую терапию, наблюдалось значительное преимущество в показателях выживаемости (медиана 70 месяцев) по сравнению с группой ЛТ (медиана 28,5 месяцев). Долгосрочные результаты зависят от стадии заболевания, наличия лимфатической инвазии, остаточной опухоли и первоначального ответа, который определялся при повторном проведении ТУР.
Важность радикальности первичного ТУР также подтверждена в японском исследовании, включавшем 82 пациентов, которым выполняли ТУР в комбинации с химиолучевой терапией [5]. Первоначальная морфологическая полная ремиссия была относительно низкой (39%) при отсутствии радикального первичного ТУР. Клинические показатели полного ответа (84%) и выживаемости (5-летняя общая 77,7%, без прогрессирования — 64,5%) были высокими, хотя некоторым больным проводилась спасительная терапия. У пациентов с первичным РМП стадии cT2 отмечалась статистически значимо более высокая выживаемость по сравнению с больными со стадией cT3-4 и рецидивным РМП.
В ряде небольших исследований была подтверждена высокая эффективность мультимодального лечения [6–9]. Показатели пятилетней общей выживаемости составили примерно 70%, хотя протоколы лечения и критерии отбора пациентов варьировались в зависимости от исследований. Прогноз для тех, кто столкнулся с рецидивами рака мочевого пузыря и переходом неинвазивного процесса в инвазивный, оказался неблагоприятным.
Низкая стадия и радикальный ТУР остаются важными прогностическими факторами. Пациентам, у которых на фоне комбинированной терапии не достигнуто полного ответа, рекомендуется выполнять раннюю цистэктомию. Примерно 40–45% больных могут прожить 4–5 лет с сохраненным мочевым пузырем [2].
Сравнения различных стратегий, направленных на сохранение мочевого пузыря и цистэктомию, показали сопоставимые показатели пятилетней выживаемости, находящиеся в диапазоне 50-60%. Тем не менее, прямые сравнительные исследования этих методов никогда не проводились, и для изучения комбинированных подходов необходим тщательный отбор пациентов [2, 10–12].
Мультимодальные стратегии сохранения мочевого пузыря требуют очень тесного взаимодействия разных специалистов и высокого уровня комплаентности пациента. Даже при достижении полного ответа на фоне мультимодальной терапии мочевой пузырь остается потенциальным источником рецидива. Примерно у половины больных можно безопасно сохранить мочевой пузырь. Важным прогностическим признаком служит отсутствие опухоли (статус Т0) при повторных ТУР первичной опухоли с проведением последующего химиолучевого лечения. Однако даже в этом случае сохраняется пожизненный риск возникновения внутрипузырных рецидивов опухоли, что требует тщательного наблюдения и осуществления множественных инвазивных процедур. Установлено, что задержка в выполнении цистэктомии из-за проведения мультимодальной терапии повышает риск поражения ЛУ на 26%, поэтому цистэктомия становится необходимой при неэффективности органосохраняющего лечения.
Как часто рак мочевого пузыря возникает вновь?
Согласно статистическим данным, частота рецидива рака мочевого пузыря составляет 50%.
Поверхностный рак мочевого пузыря составляет 80% от всех злокачественных новообразований данного органа. Уровень рецидивов этой формы варьируется от 56 до 65% на первой стадии и от 31 до 70% на второй и третьей стадиях.
Можно ли спрогнозировать рецидив рака мочевого пузыря?
С целью прогнозирования развития рецидивов рака мочевого пузыря, группа ученых, занимающаяся вопросами заболеваний мочеполовой системы Европейской организации по исследованию и лечению рака (EORTC) составила таблицы риска. С их помощью можно рассчитать вероятность повторного развития рака у конкретного пациента. В основе таблиц — база данных EORTC, включающая информацию по 2596 больным раком мочевого пузыря.
Система оценки основывается на следующих критериях:
- число опухолей;
- размер новообразования;
- предыдущие рецидивы;
- Т-критерий;
- наличие сопутствующей карциномы(CIS);
Важная информация
Нефростомия – это достаточно сложная операция, требующая высокой квалификации от хирурга и наличия высокотехнологичного оборудования в клинике. Наша операционная заставлена аппаратурой, здесь негде развернуться. Мониторы, рентген, УЗИ-аппараты, наркозное оборудование, видеокамеры и многое другое. Без этого сейчас невозможно представить себе современную работу хирурга-уролога.
Анестезиолог обеспечивает пациенту наркоз, благодаря чему он не ощущает боли в процессе операции. Мы переворачиваем пациента на бок и под контролем высокоточных УЗИ- и рентгеновских аппаратов производим пункцию почки с использованием очень тонкой иглы. Затем, с помощью специальной струны, в почку устанавливается тонкая трубочка, диаметр которой составляет всего 3-4 мм.
В конце операции с помощью цифрового рентгена производится контроль того, как установлена нефростома. Если все нормально, то с помощью одного шовчика фиксируем ее к коже. Поэтому научное название этой операции – чрескожная пункционная нефростомия или ЧПНС. В этот же день пациент может быть отпущен домой.
При каких обстоятельствах нефростомия противопоказана?
Как правило, это выраженные нарушения свертываемости крови, когда существует серьезный риск большого кровотечения. Ведь трубочка устанавливается через ткань почки и если у пациента проблемы со свертываемостью, то это может привести к беде.
Каковы достоинства проведения нефростомии в вашей медицинской практике?
Во-первых, это строго индивидуальный подход к диагностике и лечению конкретного больного. По поводу каждого пациента мы собираем консилиум, где обсуждаем именно ту тактику, которая будет для него наиболее оптимальна. Во-вторых, это колоссальный опыт в выполнении подобных процедур, более 1 000. Также огромное значение имеет поколение рентген и ультразвуковых аппаратов. В нашей клинике мы используем оборудование исключительно экспертного класса, а наши доктора прошли первичную специализацию по УЗИ.
Образ жизни при наличии нефростомы
Сексуальная активность
Функция половой системы может остаться на прежнем уровне, как и до проведения нефростомии. Главное условие — качественное опорожнение и надежная фиксация мочеприемника.
Социальная адаптация
Когда у вас есть нефростомическая трубка, это очень эмоционально непростой период. Пациенту нужно знать, что нефростома может быть удалена после того, как будет устранена причина ее установления. Образ жизни с нефростомой, конечно, меняется и отличается от обычного. Пациенту важно не замыкаться в себе, принимать поддержку своих друзей и близких. При непонятных и/или угрожающих симптомах пациент должен знать, куда ему можно обратиться за медицинской помощью.
Пациенту можно рекомендовать:
- Носить свободную, не облегающую одежду.
- Перед выходом на улицу очищать мочеприемник.
- Следить за гигиеной тела и чистотой одежды, чтобы избежать неприятных запахов.
- Тщательно фиксировать нефростомическую трубку к коже, избегая резких движений.
Многие пациенты способны жить с нефростомой на протяжении многих лет, полностью адаптируясь к изменившемуся образу жизни и оставаясь активными в социальной среде.
Когда нужно СРОЧНО обратиться к урологу?
Обязательно звоните вашему доктору:
- При повышении температуры тела без связи с сезонными ОРЗ, ОРВИ, фарингитами и др.
- При болях в области почки или установленной нефростомы.
- При наличии изменений кожи вокруг нефростомы — покраснений, отеков или гнойных выделений.
- При значительном подтекании мочи вдоль нефростомической трубки.
- При любых повреждениях нефростомической трубки.
- При изменении цвета мочи — ее малом количестве, темном цвете с неприятным запахом.
- При изменении мочи на розовый или красный цвет, наличии сгустков крови.
- Если наблюдается отсутствие выделения мочи через нефростому более двух часов.
- При выпадении нефростомической трубки.
- Если нефростомическая трубка выпала, ни в коем случае не пытайтесь установить ее на место самостоятельно.
Если у вас есть некоторые из этих симптомов, срочно обратитесь к врачу!
Опыт других людей
Алексей, 45 лет: «После операции по удалению опухоли мочевого пузыря я прошёл через непростой период восстановления. Нефростома, которая была установлена, добавила мне дискомфорта. Казалось, что каждый шаг напоминает о болезни. Но со временем я стал более оптимистично смотреть на свои грамоты. Поддержка семьи и друзей играла огромную роль в моём состоянии. Доктора говорили, что со временем ситуация улучшится, и я тоже в это верил. Я начал заниматься реабилитацией и делал всё возможное, чтобы вернуть себе нормальную жизнь.»
Мария, 38 лет: «Когда мне поставили диагноз и после удаления опухоли, я не могла поверить в то, что со мной происходит. Нефростома стала для меня не просто медицинским прибором, а постоянным напоминанием о моем состоянии. Первые недели были особенно трудными — физические боли и эмоциональные переживания. Однако, я старалась улыбаться, поддерживать связь с близкими и следовать рекомендациям врачей. Уроки йоги и психологическая помощь помогли мне справиться с тревогой. Теперь я чувствую себя гораздо лучше и стараюсь жить полной жизнью.»
Дмитрий, 52 года: «Опухоль мочевого пузыря — это серьезный удар, и когда мне сделали нефростомию, был полон тревог и сомнений. Первоначально я испытывал физическую боль и психологический дискомфорт от постоянного присутствия катетера в моей жизни. Но я понимал, что это временная мера ради здоровья. Я постоянно общался с врачами, которые объясняли мне, как правильно ухаживать за нефростомой, и это помогло мне успокоиться. Не скажу, что я забыл о болезни, но научился с ней жить, что стало для меня важным шагом к выздоровлению.»
Вопросы по теме
Какова роль психоэмоциональной поддержки в восстановлении после лечения опухоли мочевого пузыря с нефростомией?
Психоэмоциональная поддержка играет значительную роль в восстановлении пациентов после лечения опухоли мочевого пузыря. Столкнувшись с диагнозом и хирургическим вмешательством, многие пациенты испытывают страх, тревогу и депрессию. Поддержка специалистов — психологов или психотерапевтов — помогает пациентам справляться с эмоциональным состоянием, формировать позитивный взгляд на восстановление и учиться адаптироваться к новому образу жизни. Также полезной будет поддержка близких, которые могут предложить эмоциональную стабильность и ощущение заботы, что в целом способствует более успешному восстановлению.
Какие изменения в образе жизни могут потребоваться после установки нефростомы?
После установки нефростомы пациентам часто необходимо внести изменения в свой образ жизни, чтобы обеспечить комфорт и здоровье. Это может включать в себя: соблюдение диеты с низким содержанием соли, чтобы снизить нагрузку на почки; регулярный контроль за состоянием нефростомы и уретры; избегание физических нагрузок, которые могут повредить место установки; а также обязательно следить за гигиеной, чтобы избежать инфекций. Обсуждение этих изменений с врачом поможет создать индивидуальный план по восстановлению и улучшению качества жизни.
Как наладить социальные контакты после операции по удалению опухоли мочевого пузыря с нефростомой?
Налаживание социальных контактов после такой операции может быть сложной задачей, но оно крайне важно для эмоционального и психологического благополучия. Первым шагом может стать участие в группах поддержки для людей, проходящих через аналогичные испытания. Многие организации предлагают мероприятия и встречи, где пациенты могут обмениваться опытом и чувствовать себя частью сообщества. Кроме того, использование интернета и социальных сетей для общения с другими пациентами поможет расширить круг общения и уменьшить чувство изоляции.




