Очаговое образование с повышенной фиксацией флуродеоксиглюкозы (ФДГ) в онкологии является важным диагностическим маркером, указывающим на наличие злокачественного опухолевого процесса. Повышенная метаболическая активность клеток в данном образовании позволяет использовать позитронно-эмиссионную томографию (ПЭТ) для определения локализации и стадийности опухоли, а также контроля за эффективностью лечения.
Однако, следует учитывать, что повышенная фиксация ФДГ не всегда специфична для рака и может наблюдаться при воспалительных процессах или доброкачественных образованиях. Поэтому важно сопоставлять данные ПЭТ с результатами других методов исследования и клинической картины пациента для точной диагностики.
- Определение: Очаговое образование с повышенной фиксацией фДГ (Фтордезоксиглюкозы) указывает на аномальную метаболическую активность клеток, что может свидетельствовать о наличии опухоли.
- Метод исследования: ПЭТ/КТ (позитронно-эмиссионная томография с компьютерной томографией) используется для выявления участков с повышенным метаболизмом, характерным для онкологических заболеваний.
- Клинические проявления: Увеличение фиксирующих очагов может быть связано как с злокачественными, так и с доброкачественными процессами, поэтому важно проводить дифференциальную диагностику.
- Показания: Используется для стадиирования рака, оценки эффективности лечения и мониторинга рецидивов после терапии.
- Трудности интерпретации: Высокая фиксация фДГ может наблюдаться также при инфекциях и воспалительных заболеваниях, что требует осторожности в диагнозе.
Очаговое образование с повышенной фиксацией фдг в онкологии
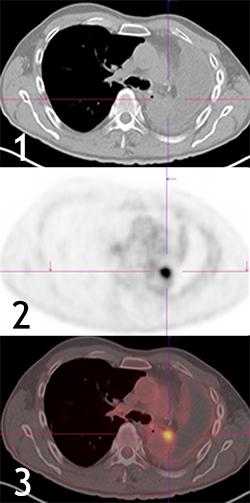
ПЭТ с фтордезоксиглюкозой (ФДГ) и рецидив рака легкого на фоне послеоперационного гидрофиброторакса:
- Изображение КТ;
- Изображение ПЭТ;
- Изображение ПЭТ/КТ
В качестве радиофармацевтического препарата (РФП), который активно применяется в клинической практике для ПЭТ-диагностики, используется 18F-фтордезоксиглюкоза (18F-ФДГ). Этот препарат занимает более 95% во всех проводимых ПЭТ-исследованиях.
С химической точки зрения 18F-ФДГ представляет собой аналог обычной глюкозы, что позволяет производить оценку гликолитической активности тканей. После внутривенного введения 18F-ФДГ аккумулируется в органах и тканях с высокой интенсивностью гликолиза, таких как головной мозг, миокард, желудок, печень и мышцы.
Принцип применения 18 F- ФДГ в онкологии основывается на разнице дифференциальных скоростей метаболизма глюкозы в доброкачественных и злокачественных тканях. Известно, что интенсивность накопления 18 F- ФДГ может быть связана с размером опухоли и может значительно варьироваться при различных типах злокачественных опухолей и (NB: накопление РФП также ускоряется при воспалительных процессах, таких как гранулемы, абсцессы, что может приводить к возникновению ложно-положительных результатов).
Многие злокачественные образования демонстрируют увеличенный метаболизм глюкозы, что делает использование ПЭТ с 18F-ФДГ высокоэффективным для диагностики. Уровень накопления 18F-ФДГ в различных опухолях указывает на степень их злокачественности и агрессивности.
При проведении противоопухолевой терапии количество жизнеспособных злокачественных клеток значительно уменьшается, что позволяет использовать количественную оценку накопления 18F-ФДГ в опухолевых структурах как чувствительный маркер эффективности терапии. Это нашло отражение в критериях оценки PERCIST (ПЭТ-реакция на лечение при солидных опухолях).
ПЭТ/КТ с применением 18F-ФДГ находит применение в диагностике, оценке стадии и динамическом наблюдении за опухолями молочной железы, колоректального рака, рака легких, рака пищевода, меланомы, лимфом и другими онкологическими заболеваниями (рекомендуем уточнять при записи на исследование). ПЭТ/КТ с 18F-ФДГ считается надежным методом для диагностики этих опухолей и определения их распространенности. Также это помогает выявлять рецидивы при наличии биомаркерного рецидива у бессимптомных пациентов, при отсутствии патологических изменений по результатам МРТ, КТ или УЗИ, а также различать рецидивы от некрозов и фиброзов, что позволяет корректировать лечение в процессе наблюдения.
- до начала лечения;
- после двух курсов химиотерапии.
Подготовка к исследованию:
- Если у вас есть сахарный диабет, пожалуйста, сообщите об этом заранее. Исследование проводится при уровне глюкозы в крови не более 8,0 ммоль/л. Если уровень глюкозы вам неизвестен, укажите это во время консультации в отделении ПЭТ;
- Сообщите нашим врачам о всех медикаментах, которые вы принимаете по рекомендации своего лечащего врача. В случае необходимости временной отмены медикаментов перед исследованием, необходимо обсудить это с вашим лечащим врачом;
- Сообщите о возможных аллергиях на препараты йода или анальгетики;
- Если у вас есть сложности с неподвижным положением на спине 20-30 минут с поднятыми руками, дайте знать до начала исследования;
- Избегайте физических нагрузок за день-два до исследования;
- Накануне разрешается легкий ужин без продуктов, богатых углеводами (кондитерские изделия, хлеб, фрукты). После ужина разрешается только пить теплую воду без сахара и газа;
- В день исследования приходите натощак и выпейте не менее 0,5 литра теплой воды без газа и сахара;
- В холодное время года позаботьтесь о теплом варианте одежды – это снизит риск накопления РФП в бурой жировой ткани.
Оценка эффективности лечения лимфомы ходжкина на раннем этапе, распространенность заболевания: 1) до лечения; 2) после 2-х курсов ПХТ.
- Если у вас есть диабет, пожалуйста, сообщите заранее. Проверьте уровень сахара в крови, чтобы он не превышал 7 ммоль/литр;
- Если вы принимаете какие-либо лекарства, обязательно обсудите это с врачом на первичной консультации, так как может возникнуть необходимость их временной отмены, в таком случае нужна консультация вашего лечащего врача;
- Избегайте физических нагрузок за два дня до исследования;
- За день до исследования пейте больше негазированной воды без сахара, а накануне вечера избегайте жирной и углеводной пищи, не принимайте лекарства от простуды, не курите, не употребляйте алкоголь, не жуйте жевательную резинку;
- Исследование проводится строго натощак!
Подготовка к исследованию
В случае наличия сахарного диабета у ребенка, это должен учитывать врач, назначающий ПЭТ/КТ. Исследование возможно при уровне глюкозы в крови не более 8,0 ммоль/л непосредственно перед процедурой.
Обязательно сообщите врачам, проводящим исследование, о медикаментах, которые принимает ваш ребенок. Если потребуется временная отмена препаратов перед процедурой, необходимо согласовать это с лечащим врачом.
Противопоказанием могут служить аллергические реакции на препараты йода или обезболивающие средства. Необходимо максимально сократить физические нагрузки ребёнка за 1-2 дня до исследования. Накануне перед исследованием ребёнку разрешается легкий ужин без продуктов, содержащих в больших количествах углеводы (кондитерские и мучные изделия, фрукты). После ужина можно пить только теплую воду без сахара и газа.
Исследование проводится натощак, с необходимым объемом теплой воды без газа и сахара от 150 до 500 мл.
В холодное время года ребенку следует надеть теплую одежду, чтобы снизить возможность накопления РФП в буром жире. Длительность процедуры составляет от двух до трех часов. Маленьким детям она может быть проведена под общей анестезией.
ПЭТ с фторэтилтирозином
Фторэтилтирозин (18F-ФЭТ) — полунезаменимая аминокислота, меченая изотопом [18F] с периодом полураспада 109 мин.
Опухолевые клетки активно делятся, и для их функционирования необходим синтез белка из аминокислот. Для большинства опухолевых клеток характерно усиление транспорта аминокислот из внешней среды в клетку и в обратную сторону.
18F-ФЭТ показывает уровень активности аминокислотного транспорта внутри клетки и обладает высокой диагностической точностью при определении объема опухолевого поражения и оценке границ при планировании хирургического или лучевого лечения.
Из организма тирозин и 18F-ФЭТ транспортируются с помощью L-аминокислотных транспортеров. Слабое физиологическое накопление РФП в неизмененном веществе головного мозга значительно увеличивает чувствительность в выявлении образований. Длительный период полураспада позволяет проводить многослойные исследования или динамическое наблюдение.
Позитронно-эмиссионная томография в дифференциальной диагностике очаговых образований печени
Очаговые образования в печени являются одной из важных проблем современной лучевой диагностики в онкологии и хирургии. Особенно это актуально для пациентов, имеющих отягощенный анамнез по колоректальному раку и циррозу печени. Выживаемость больных в основном определяется наличием или отсутствием отдаленных метастазов. У большинства этих больных поражение печени является первым признаком распространенности поражения. Поэтому скрининговые обследования на предмет поиска метастазов являются предпосылкой для планирования дальнейшего лечения и наблюдения за больным.

Очаговые образования в печени представляют собой одну из серьезных задач современной радиодиагностики в области онкологии и хирургии. Каждый год в мире регистрируется 1-1,2 миллиона случаев колоректального рака. У 50–60% таких пациентов в дальнейшем развиваются метастазы.
У значительного числа пациентов (до 80-85%) обнаруживаются метастазы в печени, и у половины из них печень становится единственным органом, куда происходят метастазирования. Выживаемость данной группы пациентов напрямую зависит от наличия метастазов. В большинстве случае поражение печени выявляется как первый признак прогрессирования заболевания. Поэтому скрининговые обследования направленные на выявление метастатических повреждений, необходимы для планирования последующего лечения и наблюдения за пациентом.
Пациент М. Оперирован по поводу колоректального рака 1,5 года назад. При КТ и УЗИ выявлены очаговые образования печени (Рис. 1а). При ПЭТ исследовании — изолированное метастатическое поражение печени (Рис. 1б).
Необходимость хирургического удаления метастазов печени была доказана, поскольку 5-летняя выживаемость пациентов при лечении химиотерапией не превышает 5%, а без такого лечения – всего 1%. В то же время, радикальная резекция печени позволяет 35-40% пациентов продлить жизнь на 5 и более лет.
При предоперационной оценке состояния пациента крайне важна оценка распространенности заболевания и степени злокачественности выявляемых образований. Для обследования проводятся компьютерная томография печени, рентгенография легких и определение уровня раково-эмбрионального антигена. Для оптимизации оперативной тактики полезно использовать компьютерную томографию печени с контрастом печеночной артерии, так как метастазы получают кровоснабжение преимущественно через a. hepatica, в отличие от нормальной ткани, которая получает его через v. porta. Эффективно также применение интраоперационного УЗИ печени, что позволяет выявлять ранее не распознанные метастазы в 15-25% случаев.
Пациент В. При КТ (Рис. 2а) выявлено объемное образование печени, подозрительное на метастатическое поражение. При проведении ПЭТ (Рис. 2б) подтверждена злокачественная природа выявленного образования, а также обнаружено метастатическое поражение лимфоузлов ворот печени и средостения.
Еще одной актуальной проблемой современной онкологии является первичный рак печени, возникающий на фоне цирроза. Это связано с возможностью диагностирования даже небольших очаговых образований печени на ранних стадиях с использованием новейших методов.
По приблизительным данным, в мире каждый год фиксируют более 500000 новых случаев рака печени. Известно, что цирроз печени является «благоприятной средой» для развития гепатоцеллюлярного рака (ГЦР). ГЦР, развивающийся на фоне цирроза, становится серьезной проблемой здравоохранения в разных странах. В среднем, опухоль диаметром до 2 см формируется за период от 4 до 12 месяцев.
При циррозе печени примерно 50% узлов диаметром менее 1 см оказываются не опухолевыми. Наличие фиброза, регенераторных узлов и участков некроза создаёт сложный и неоднородный паттерн паренхимы печени, что значительно усложняет диагностику злокачественных образований. Особенно трудно отличить регенераторные узлы от других очаговых формирований в печени. Согласно данным исследования Bolondi, Sofia и др. (2001), гепатоцеллюлярная карцинома (ГЦР) чаще всего приводит к летальному исходу у пациентов с циррозом. Любое новое образование печени у таких больных в первую очередь вызывает подозрение на ГЦР. Однако следует учитывать, что образования при циррозе имеют атипичные характеристики и могут имитировать узлы регенерации, так как они тоже получают кровоснабжение через ветви печеночной артерии и накапливают контраст, аналогично ГЦР.
Давно изучены семиотика гепатоцеллюлярного рака, характер контрастирования опухоли, косвенные признаки, но все это, к сожалению, не позволяет с уверенностью диагностировать цирроз-рак, если размер опухоли менее 2 см, при этом ранняя диагностика ГЦР крайне важна, так как увеличивается вероятность благоприятного результата после резекции или трансплантации печени.
Пациент Г. На УЗИ (Рис. 3а) было обнаружено очаговое образование печени, расцененное как доброкачественное. Однако при выполнении КТ с контрастом (Рис. 3б) характер этого образования не позволял исключить возможность злокачественного процесса. ПЭТ-исследование (Рис. 3в) подтвердило наличие объемного новообразования злокачественного характера (ГЦР).
Следующей проблемой лучевой диагностики, хирургии и онкологии являются образования печени, обнаруженные случайно. В этом случае необходима дифференциальная диагностика выявленных очагов во избежание ненужных лечебных мероприятий и хирургических вмешательств, а получение неинвазивными методами надежных характеристик образований печени стало почти так же важно, как и само обнаружение этих образований.
Пациент Д. При проведении КТ (Рис. 4а) и УЗИ (Рис. 4б) были выявлены очаги печени с неопределённой этиологией. Однако результаты ПЭТ (Рис. 4в) исключили злокачественное поражение.
Диагноз: цирроз печени. Регенераторные узлы.
В современном арсенале врачей есть большое количество диагностических методик, позволяющих установить диагноз. И в настоящее время все большее значение в диагностической практике приобретает позитронно-эмиссионная томография (ПЭТ). Не стоит рассматривать ПЭТ изолированно от других методов исследования, поскольку, только комплексный диагностический подход может дать наиболее полную картину заболевания.
Позитронно-эмиссионная томография, несмотря на свои специфические особенности и ограничения, заняла важное место в диагностической стратегии изучения пациентов, так как позволяет осуществлять функциональный анализ биохимических процессов на молекулярном уровне в режиме томографии.
Наибольшее распространение в онкологии получили исследования с использованием 18F-фтордезоксиглюкозы (ФДГ), что позволяет отслеживать углеводный обмен. Суть метода основана на том, что злокачественные клетки непропорционально увеличивают потребление глюкозы, благодаря чему увеличивается усвоение ФДГ в опухолевой ткани по сравнению с нормальными клетками. Активность гликолиза в злокачественных образованиях зависит от их степени злокачественности. Кроме того, у злокачественных клеток наблюдается высокая активность гексокиназы и пониженная активность фосфатазы. Образующийся 18F-ФДГ-6-фосфат не подлежит дальнейшим реакциям гликолиза, создавая «метаболическую ловушку», которая приводит к увеличению его концентрации в тканях опухоли и упрощает их выявление.
В некоторых случаях традиционные методы лучевой диагностики, такие как УЗИ, РКТ и МРТ, не дают чёткой интерпретации морфологии обнаруженных очагов в печени, особенно при циррозе. ПЭТ позволяет оценить биологическую активность этих очагов, а также отслеживать изменения во время лечения и выявлять регионарные и отдалённые метастазы в ходе одного исследования. Данная процедура является минимально инвазивной, требует лишь внутривенной инъекции и позволяет без травмировать выявить злокачественные образования.
Нами было обследовано 90 пациентов с очаговыми поражениями печени.
КТ была проведена на аппарате компании Siemens «Somatom Plus 4» в спиральном режиме с болюсным контрастированием. У всех изученных пациентов были обнаружены очаговые образования различной формы и размеров в печени, которые в разной степени накапливали контрастный препарат в артериальной и венозной фазах.
УЗИ выполнялось на аппарате «Sonoline Elegra» фирмы Siemens с использованием датчика 3,5 MHz. УЗИ подтвердило наличие объемных образований в печени у 94% пациентов. В 6% случаев изменений паренхимы печени не обнаружили.
ПЭТ обследование осуществлялось на томографе «ECAT EXACT 47» фирмы Siemens с использованием 18F-ФДГ. Сканирование проводилось в статическом режиме по протоколу Whole body в режиме 2D. Обработка полученных данных включала в себя визуальную оценку изображения «всего тела» пациента, а также измерение коэффициента дифференциального накопления ФДГ в выявленных очагах.
В результате у 37% пациентов не были найдены очаги с повышенным захватом ФДГ в печени. При проведении последующих гистологических исследований у этих пациентов был подтвержден диагноз цирроза. 6% пациентов продемонстрировали очаги гиперфиксации ФДГ, которые не визуализировались на УЗИ и странным образом изменили свои характеристики при КТ. Гистологическое исследование подтвердило наличие гепатоцеллюлярного рака у данной группы.
54% пациентов имели в печени очаги с высоким уровнем накопления ФДГ, которые по размерам и расположению соответствовали объемным образованиям, выявленным при КТ и УЗИ. При этом в 44% случаев, помимо участков с гиперфиксацией в печени, были найдены множественные внепеченочные очаги с повышенным накоплением препарата, что указывает на генерализацию опухолевого процесса.
У 3% изолированные очаги гиперфиксации ФДГ при ПЭТ определялись в печени, количественно больше чем при КТ и УЗИ исследованиях. Количество очагов, их расположение и отсутствие накопления ФДГ в регионарных лимфоузлах и других органах позволило провести хирургическое лечение с последующим гистологическим исследованием, при котором было подтверждено количество выявленных очагов и их метастатическая природа.
Таким образом, Позитронно-эмиссионная томография проявила себя как высокоэффективный метод для выявления метастазов в печени и их дифференциальной диагностики от доброкачественных новообразований. С помощью ПЭТ возможно Выявление внепеченочных метастазов, что влияет на стадию заболевания и позволяет корректировать лечение и планирование хирургического вмешательства. Этот метод позволяет неинвазивно оценить степень заболевания печени и других органов за одно исследование, тем самым сокращая время диагностики.
Применение ПЭТ становится необходимым при диагностике пациентов с очаговыми образованиями печени, несмотря на высокие затраты на исследование.
Очаговое образование с повышенной фиксацией ФДГ (фтордезоксиглюкозы) является важным диагностическим показателем в онкологии. Оно возникает, когда клетки опухоли поглощают радиофармацевтическое вещество, что свидетельствует о повышенном метаболизме. В большинстве случаев такая повышенная фиксация наблюдается в злокачественных новообразованиях, и её наличие требует тщательного обследования для уточнения диагноза и определения дальнейшей тактики лечения.
При интерпретации данных ПЭТ/КТ с фиксированием ФДГ критически важно учитывать различные факторы. Например, воспалительные процессы, инфекции или даже доброкачественные опухоли могут также привести к повышенной радиофиксации. Поэтому необходимо провести дифференциальную диагностику, чтобы не поставить неправильный диагноз. Важно помнить, что одно только наличие очагового образования с повышенной фиксацией ФДГ не является достаточным основанием для conclusively определения злокачественности.
Наиболее часто подобные образования встречаются в органах, подверженных высоким метаболическим нагрузкам, таких как легкие, печень и лимфатические узлы. Поэтому, для более точного диагноза и избежания ложноположительных результатов, требуется использование дополнительных методик, таких как биопсия или магнитно-резонансная томография. Комплексный подход к этому вопросу значительно повышает шансы на правильную диагностику и успешное лечение пациентов с онкологическими заболеваниями.
ПЭТ в дифференциальной диагностике очаговых образований печени у больных колоректальным раком
Очаговые образования в печени являются одной из важных проблем современной лучевой диагностики в онкологии и хирургии. В мире колоректальным раком ежегодно заболевает 1–1,2 млн. человек. У 50–60% пациентов с течением времени развиваются метастазы. У большей части из них (до 80–85%) имеются метастазы в печень, а у половины из этого числа печень является единственным органом метастазирования. Выживаемость этой группы больных определяется наличием или отсутствием отдаленных метастазов.
У большинства больных поражение печени нередко становится первым сигналом о распространении заболевания. Поэтому скрининг для выявления метастатического поражения крайне важен для планирования последующего лечения и наблюдения за пациентами.
Для оценки возможности хирургического вмешательства критически важно предварительно оценить распространение болезни и определить злокачественность обнаруженных очагов. В ходе диагностики обязательно нужно проводить КТ печени, рентгенографию легких и определять уровень раково-эмбрионального антигена (РЭА). Для лучшего выбора тактики операции полезно выполнить КТ печени с контрастированием печеночной артерии, так как известно, что в отличие от нормальной печеночной ткани, метастазы получают питание преимущественно из печеночной артерии. Также необходимо проведение интраоперационного УЗИ печени, поскольку нераспознанные ранее метастазы могут быть идентифицированы в 15-25% случаев.
В современном арсенале врачей есть большое количество методик, позволяющих установить диагноз. И в настоящее время все большее значение в диагностической практике приобретает позитронно-эмиссионная томография (ПЭТ). Не стоит рассматривать ПЭТ изолированно от других методов исследования, поскольку, только комплексный диагностический подход может дать наиболее полную картину заболевания.
Позитронно-эмиссионная томография, несмотря на ее специфические особенности и ограничения, уверенно заняла своё место в диагностическом процессе. Этот функциональный метод исследует биохимические процессы на молекулярном уровне в режиме томографии.
Иногда традиционные методы лучевой диагностики (УЗИ, РКТ, МРТ) не позволяют однозначно интерпретировать морфологическую структуру выявленных очагов в печени. ПЭТ успокаивает эту проблему, предоставляя возможность оценить биологическую активность этих образований, динамику их изменений в процессе терапии, а Выявить регионарное и отдалённое метастазирование в ходе одного исследования. Она является минимально инвазивной процедурой, требующей лишь внутривенной инъекции для безболезненного выявления злокачественных новообразований.
Нами было обследовано 138 пациентов с очаговыми поражениями печени.
КТ была выполнена на томографе “Somatom Plus 4” компании Siemens в спиральном режиме с применением болюсного контрастирования. Все пациенты продемонстрировали различные по форме и размеру очаговые образования в печени, которые накапливали контрастный препарат в артериальной и последующих стадиях.
УЗИ брюшной полости проводилось с использованием аппарата “Sonoline Elegra” фирмы Siemens с датчиком 3,5 MHz. На УЗИ было отметили наличие объемных образований в печени у 94% пациентов. У 6% наблюдений изменений в паренхиме печени не обнаружили.
Для ПЭТ-исследования использовался томограф “ECAT EXACT 47” от компании Siemens с применением 18F-ФДГ.
Сканирование проводилось в статическом режиме по протоколу Whole body в режиме 2D. Обработка полученных данных включала в себя визуальную оценку изображения всего тела пациента, измерение стандартизованного уровня накопления (SUV), а также измерение коэффициента дифференциального накопления ФДГ в выявленных очагах.
В результате у 32% пациентов в печени не были найдены очаги с повышенным захватом ФДГ. При последующем гистологическом исследовании у этих больных был подтвержден диагноз цирроза. У 8% пациентов выявили очаги гиперфиксации ФДГ, которые не визуализировались на УЗИ и странным образом изменяли свои характеристики при КТ. Гистологическое исследование показало, что у данной группы пациентов диагностирован гепатоцеллюлярный рак.
У 56% обследованных были выявлены очаги в печени с высоким уровнем накопления ФДГ, размеры и расположение которых соответствовали объемным образованиям, зафиксированным при КТ и УЗИ. Из них в 46% случаев, помимо участков гиперфиксации в печени, смогли обнаружить множественные внепеченочные очаги с повышенным накоплением препарата, что указывает на генерализацию опухолевого процесса.
У 4% изолированные очаги гиперфиксации ФДГ при ПЭТ определялись в печени, количественно больше чем при КТ и УЗИ исследованиях. Количество очагов, их расположение и отсутствие накопления ФДГ в регионарных лимфоузлах и других органах позволило провести хирургическое лечение с последующим гистологическим исследованием, при котором было подтверждено количество выявленных очагов и их метастатическая природа.
Таким образом, ПЭТ доказала свою высокую эффективность в обнаружении метастазов в печени и в дифференциальной диагностике с доброкачественными очаговыми образованиями. Метод ПЭТ также дает возможность выявлять внепеченочные метастазы, что меняет стадию заболевания и открывает путь для корректировки проводимого лечения и планирования хирургического вмешательства. ПЭТ позволяет неинвазивно оценить степень поражения печени и других органов единовременно, что существенно ускоряет процесс диагностики.
Очаговое образование с повышенной фиксацией фдг в онкологии
ПЭТ/КТ с 18F-ФДГ в настоящее время — это наиболее распространённая и усовершенствованная методика в области радиоизотопной диагностики.
Метод основан на потребности злокачественных клеток в универсальном источнике энергии, которым является глюкоза. Для ПЭТ/ КТ используют аналог природной глюкозы, 18F—фтордезоксиглюкоза, в которой одна из составных частей молекулы замещена изотопом 18 – F, таким образом молекула становится «меченной».
После внутривенного введения 18F-ФДГ он начинает накапливаться в органах и тканях с разной интенсивностью. Физиологически данный радиоизотоп активно усваивается в тех органах и тканях, где происходит активный обмен глюкозы, таких как головной мозг, миокард, печень и мышцы.

Позиционная эмиссионная томография с компьютерной томографией (ПЭТ/КТ), использующая 18-ФДГ, на сегодняшний день является ведущим и наиболее используемым способом в области радиоизотопной диагностики.
Данная методика основывается на высокой потребности злокачественных клеток в источнике энергии, которым служит глюкоза. Для ПЭТ/КТ применяется аналог естественной глюкозы — 18F-фтордезоксиглюкоза, где атом углерода в молекуле замещен на изотоп 18-Ф, что делает молекулу «меченной».
При внутривенном введении 18F– ФДГ начинает с различной интенсивностью накапливаться в органах и тканях. Физиологически 18F – ФДГ интенсивно накапливается в органах и тканях, в которых активно протекает метаболизм глюкозы (головной мозг, миокард, печень, мышцы).
Основной принцип применения 18F-ФДГ заключается в различии темпов метаболизма глюкозы между нормальными и опухолевыми тканями.

Злокачественные клетки демонстрируют более активный рост и деление, что требует от них значительного количества глюкозы, в результате чего они быстрее накапливают 18F-ФДГ. Важно также отметить, что уровень накопления радиофармацевтика может значительно колебаться в зависимости от разновидности опухоли.
Таким образом, опухолевые клетки активно захватывают 18 F – ФДГ и далее в клетке он подвергается распаду с выделением энергии, которую фиксируют детекторы аппарата ПЭТ/КТ, с построением изображений, которые и оценивает врач. Соответственно, чем выше уровень потребности опухолевой клеткой в глюкозе, тем активнее происходит захват 18F – ФДГ, тем больше энергии выделяется при распаде изотопа 18F, тем «ярче» изображения оцениваемые врачом.
Злокачественные клетки демонстрируют более активный рост и деление, что требует от них значительного количества глюкозы, в результате чего они быстрее накапливают 18F-ФДГ. Важно также отметить, что уровень накопления радиофармацевтика может значительно колебаться в зависимости от разновидности опухоли.
Злокачественные клетки демонстрируют более активный рост и деление, что требует от них значительного количества глюкозы, в результате чего они быстрее накапливают 18F-ФДГ. Важно также отметить, что уровень накопления радиофармацевтика может значительно колебаться в зависимости от разновидности опухоли.
Определение стадии рака легкого при ПЭТ
ПЭТ-КТ используют перед началом радикального лечения у клинически соответствующих пациентов с раком легких. Исследование PLUS показало, что при проведении ПЭТ пациентам в рамках предоперационного обследования число неэффективных торакотомий было на 50% меньше, чем у больных, которым проводили только КТ.
Степень поглощения опухолевой ткани частично зависит от ее размера и типа клеток. Мелкоклеточный рак легких (МРЛ) является самым активным в аспекте накопления ФДГ.
Главная задача ПЭТ/КТ перед началом радикального лечения — провести оценку структур средостения и выявить наличие метастазов. Также данный метод демонстрирует прогностическую ценность. Были определены значительное количество дополнительных отклонений, выявляемых при использовании ПЭТ/КТ у пациентов с предполагаемым или подтвержденным морфологически раком легких.
Оценка структур средостения на ПЭТ при раке легкого
Информативность ПЭТ с использованием ФДГ зависит от размеров лимфатических узлов и вероятных других причин, которые могут привести к повышению поглощения препарата, например, гранулематоз. Метаанализ по этому вопросу показал, что при наличии лимфатических узлов размером 10-15 мм на КТ и отрицательной ПЭТ вероятность наличия ракового образования составляет 5%, в то время как при размерах более 16 мм этот показатель возрастает до 21%.
Ложноположительные результаты исследования зависят от распространенности сопутствующего гранулематоза. Согласно опубликованным данным, чувствительность и специфичность варьируют в пределах 61-86 и 73-96%.

Значение ПЭТ в мониторинге онкологических заболеваний
ПЭТ играет ключевую роль в оценке эффективности лечения и динамическом мониторинге пациентов с онкологическими заболеваниями. Основные преимущества метода заключаются в следующем:
- Оценка ответа опухоли на химиотерапию или лучевую терапию;
- Раннее выявление рецидивов на фоне рубцовых изменений;
- Определение прогрессирования с появлением новых метастатических очагов.
Для наблюдения используется параметр динамики SUV. Его снижение (более 25%) свидетельствует о положительном эффекте лечения, тогда как увеличение SUV указывает на прогрессирование заболевания.
Дифференциальная диагностика рецидива и лучевого некроза
Сложность может представлять дифференциальная диагностика местного рецидива опухоли и лучевого некроза окружающих тканей после лучевой терапии. В таких случаях также используется анализ динамики метаболической активности по данным ПЭТ:
- При лучевом некрозе наблюдается снижение накопления ФДГ в облученной области;
- Рецидив опухоли проявляется увеличением метаболической активности в соответствующем участке.
Эти данные помогают избежать ненужных хирургических вмешательств или корректировки лечения.
Опыт других людей
Алексей, 35 лет, инженер. У меня была мысль о том, что если появляются какие-то необъяснимые симптомы, то лучше не игнорировать их. При обследовании у меня обнаружили очаговое образование с повышенной фиксацией фДГ. Я был сильно напуган, так как в нашей семье были случаи рака. Врач объяснил, что это может быть связано как с доброкачественными, так и с злокачественными образованиями. После длительного наблюдения и дополнительных анализов, оказалось, что это доброкачественное образование. Я осознал важность регулярных обследований и своевременной диагностики.
Мария, 28 лет, врач. На практике я сталкивалась с пациентами, у которых были выявлены очаговые образования с повышенной фиксацией фДГ. Это всегда вызывало у меня большое беспокойство, так как такие результаты могут указывать на серьезные онкологические заболевания. Один из моих пациентов, мужчина среднего возраста, не придавал значения своим симптомам, пока не прошел обследование. Обнаружение таких образований стало для него шоком, но благодаря ранней диагностике мы смогли начать лечение вовремя. Это подтверждает, насколько важно внимание к своему здоровью.
Сергей, 50 лет, предприниматель. Моя история началась с обычной усталости и потери веса. Когда на ультразвуковом исследовании мне сказали о наличии очагового образования с повышенной фиксацией фДГ, я был в замешательстве. Мне сообщили, что необходимо провести ряд дополнительных исследований. Это было очень тяжелое время, полное тревог и раздумий. После подтверждения диагноза рак, я понял, что мне нужно бороться. Благодаря поддержке семьи и правильному выбору лечения, сейчас я на пути к выздоровлению. Это научило меня ценить каждый момент жизни и обращать внимание на свое здоровье.
Вопросы по теме
Что такое очаговое образование с повышенной фиксацией ФДГ и как оно диагностируется?
Очаговое образование с повышенной фиксацией ФДГ (фтордезоксиглюкозы) — это область ткани, где происходит повышенное поглощение радиоактивной глюкозы, что может указывать на метаболическую активность, характерную для опухолевых процессов. Такие образования чаще всего выявляются с помощью позитронно-эмиссионной томографии (ПЭТ), в которой используется ФДГ как радиофармацевтический препарат. Повышенная фиксация чаще всего наблюдается при наличии злокачественных опухолей, однако может встречаться и при доброкачественных процессах, таких как воспаление или инфекция.
Каковы возможные причины повышения фиксации ФДГ, кроме онкологии?
Повышенная фиксация ФДГ не всегда свидетельствует о наличии злокачественной опухоли. Существует множество причин, которые могут вызвать аналогичный эффект. К таким причинам относятся инфекционные процессы (например, пневмония или остеомиелит), воспалительные заболевания (такие как артрит или хронические воспалительные состояния), а также метаболические нарушения и некоторые доброкачественные образования, такие как аденомы. Поэтому интерпретацию результатов ПЭТ необходимо проводить в контексте других клинических данных и исследований.
Каковы перспективы использования ФДГ для мониторинга лечения онкологических заболеваний?
Использование ФДГ в ПЭТ-обследованиях предоставляет ценные данные для мониторинга эффективности лечения онкологических заболеваний. Поскольку ФДГ позволяет визуализировать метаболическую активность опухоли, его применение может помочь в раннем обнаружении ответа на терапию: снижение фиксации ФДГ может указывать на уменьшение опухоли или ее метастазов. Однако необходимо учитывать, что интерпретация таких изменений требует комплексного подхода и дообследования. В будущем ожидается развитие новых радиофармацевтиков и методов визуализации, что позволит повысить точность диагностики и мониторинга в онкологии.




