Статья носит информационный характер, не является индивидуальной медицинской рекомендацией. Имеются противопоказания, необходима консультация специалиста.
Фтор — единственный галоген, который входит в состав зубной эмали. Он играет ключевую роль в защите зубов от разрушения и кариеса.
В следующих разделах статьи мы поговорим о том, как фтор влияет на здоровье зубов, как правильно использовать фторсодержащие продукты для укрепления эмали, и какие другие методы помогут сохранить зубы здоровыми на долгие годы.
- Фтор
Зубная эмаль состоит из кристаллических элементов, среди которых наиболее важную роль играет фтор. Фториды встраиваются в кристаллическую решетку зубной эмали, делая её более устойчивой к разрушению и помогая предотвратить образование кариеса. Этот процесс называется фторированием и является одним из эффективных методов профилактики зубных заболеваний.
4-буквенный галоген, часть зубной эмали
Найдено 63 альтернативных определения слова "фтор":
- Слова с буквой "ф"
- Слова, заканчивающиеся на "р"
- Слова, содержащие "фт"
- Слова, оканчивающиеся на "ор"
- Слова, содержащие "фто"
- Слова, заканчивающиеся на "тор"
- Составить слова из букв слова "фтор"
В поисках таинственного "фтора"
В периодической таблице Менделеева девятый элемент — фтор, вместе с хлором, бромом, йодом и астатом, относится к группе галогенов, которые все являются активными окислителями. Среди них фтор является самым агрессивным и поэтому может встречаться в природе только в соединениях. Взаимодействие этого элемента с другими веществами обычно сопровождается воспламенением и даже взрывом. Химики много лет упорно пытались получить чистый фтор, но это оказалось самой трудной экспериментальной задачей в истории химии.
Один из ученых, которые пытались получить чистый фтор — Карл Вильгельм Шееle. Однако сейчас Анри Муассан проводит эксперимент по получению этого элемента в своей лаборатории. Он использовал устройство с двумя электродами, выполненными из платины, расположенные в U-образной трубке, где залита смесь HF и KF. Устройство было помещено в сосуд для охлаждения. При пропускании тока на аноде выделяется фтор, а на катоде — водород.
При температурах ниже 120К (–153°С), фтор имеет желтую жидкую форму, а при обычных условиях – газ без цвета. Однако при больших скоплениях он может принимать зеленовато-желтый оттенок.
Негативное влияние иммунной системы на процесс разрушения зубов

1 июля, 2019
Формирование зубной эмали
У всех хищных животных, включая человека, природой предусмотрены острые зубы с прочной эмалью, которые гарантируют выживание. У человека зубы начинают формироваться еще в утробе матери. Крепкая эмаль молочных зубов и затем постоянных зубов формируется благодаря полноценному питанию матери во время беременности и грудного вскармливания, а также употреблению комплексных витаминов и минералов. К сожалению, в современных магазинах продукты зачастую не содержат необходимых питательных веществ.
Процесс формирования зуба начинается с вершины коронки и простирается по всей длине до корня как дентина, так и эмали. После рождения младенца корневая часть зуба начинает постепенно удлиняться, что приводит к появлению молочных зубов примерно в шести месяцев. Молочные зубы не обладают такой же прочностью, как постоянные, из-за того, что их эмаль менее прочная и быстрее разрушается, особенно при постоянном потреблении сладостей. Важно начинать уход за полостью рта ребенка с самого начала жизни.
Зубная эмаль представляет собой твердую внешнюю оболочку зубов, состоящую главным образом из гидроксиапатита. Среди химических элементов, входящих в состав зубной эмали, особенно важными являются кальций, фосфор и фтор.
Фтор играет ключевую роль в процессе минерализации зубной эмали и защите от кариеса. Он способствует образованию фторапатита, который повышает стойкость зубов к разрушению под воздействием кислот. Поступление фтора в организм может осуществляться как с пищей, так и через применение фторсодержащих зубных паст и прополосков.
Таким образом, для укрепления зубной эмали и профилактики кариеса рекомендуется поддерживать оптимальный уровень фтора в организме, а также использовать фторсодержащие средства гигиены полости рта. Регулярные посещения стоматолога также позволят вовремя выявить и предотвратить различные проблемы с зубами и зубной эмалью.
Восстановление эмали зубов
К сожалению, из-за особенностей строения эмали, естественная регенерация поврежденных тканей зубов невозможно. Однако, это не означает, что зубы нельзя восстановить.
Для лечения небольших повреждений стоматологи часто используют фторсодержащие препараты, такие как гели и лаки. Они не восстанавливают эмаль, но делают ее более прочной и устойчивой к воздействию внешних факторов. Такие препараты наносятся на поврежденную эмаль тонкой кисточкой в кабинете стоматолога, а некоторые можно использовать и дома. Однако, перед назначением лечения пациент обязательно должен получить консультацию и рекомендации врача.
Если эмаль зуба серьезно повреждена, фосфат кальция в аморфном состоянии используется для ее восстановления. При контакте с зубом, данный вещество проходит химическую реакцию и превращается в апатит, который в составе структуры напоминает апатиты эмали. В результате этого применения эмали восстанавливают свой прежний вид, что не только устраняет дефект, но и снимает повышенную чувствительность зуба, а также делает его более эстетичным.
Информация о происхождении иода
Иод был впервые выделен из золы морских водорослей французским химиком Б. Куртуа в 1811 году при помощи концентрированной H2SO4. Название элемента произошло от греческого слова ἰώδης, что означает "фиолетовый" и связано с цветом паров иода.
Содержание иода в земной коре составляет 4·10 -5 % по массе. Элемент в основном находится в морской воде и морских водорослях, а В нефтяных буровых водах. Он Входит в состав минералов, таких как лаутарита Ca(IO3)2 — природный иодид и иодат.
Характеристики

Настройка внешней электронной оболочки атома иода имеет следующий вид: 5s 2 5p 5. В соединениях иод может проявлять различные степени окисления – от минус одного до плюс семи, а электроотрицательность его составляет 2,66 по шкале Полинга. Атомный радиус иода равен 140 пикометров, в то время как радиус ионов I– составляет 206 пикометров, а для ионов I5+ – 109 пикометров.
Иод может находиться в жидком и газообразном состоянии в виде паров и жидкости. Молекулы иода, существующие в газообразном и жидком состоянии, представляют собой двухатомные молекулы I2. Обратим внимание, что заметная диссоциация (около 3%) молекул I2 на атомы происходит при температуре выше 800℃ и под воздействием света. Стоит отметить, что молекулы I2 диамагнитны.
Iод является наименее химически активным галогеном и не взаимодействует непосредственно с благородными газами, кислородом, серой, азотом и углеродом.
При нагревании иод взаимодействует с металлами, создавая иодиды металлов, например иодид алюминия (AlI3), фосфором (иодид фосфора PI3), водородом (иодоводород HI) и другими галогенами, образуя так называемые межгалогенные соединения. В отличие от хлора и брома, иод является менее сильным окислителем, имеющим скорее восстановительные свойства. Хлор окисляет иод до иодноватой кислоты (HIO3): I2 + 5Cl2 + 6H2O = 2HIO3 + 10HCl.
Реакция: 2 иода + 5 хлоров + 6 воды = 2 иодноватистой кислоты + 10 соляной кислоты. Иод может образовывать различные кислоты с кислородом, соответствующие различным степеням окисления: иодноватистую (со степенью окисления +1) соли которой являются гипоиодиты (например, гипоиодит калия KIO), иодноватую (со степенью окисления +5) соли которой являются иодаты (например, иодат калия KIO3), периодическую (или метаиодную) кислоту HIO4 и ортопериодическую (или ортоиодную) кислоту H5IO6 (со степенью окисления +7). Соли этих кислот являются метапериодаты (например, метапериодат калия KIO4), ортопериодаты (например, дигидроортопериодат калия K3H2IO6) и периодаты (общее название для солей кислот, содержащих иод со степенью окисления +7). Кислородсодержащие кислоты и их соли обладают окислительными свойствами.
HIO является слабой кислотой, и она существует только в водных растворах. Гипоиодиты также существуют только в водных растворах и образуются при взаимодействии иода с растворами щелочей. HIO3 — безцветный кристаллический материал, хорошо растворяющийся в воде с температурой плавления 110 градусов Цельсия; когда нагревается до 300 градусов Цельсия, HIO3 отщепляет воду и образует кислотный оксид I2O5.
Можно получить HIO3, окисляя иод дымящей азотной кислотой (3I2 + 10HNO3 = 6HIO3 + 10NO + 2H2O). Иодаты — это кристаллические материалы, растворимые в воде, которые получаются при взаимодействии иода с горячими растворами щелочей. При нагревании иодаты разлагаются, например, 4KIO3 = KI + 3KIO4, при нагревании выше 400 градусов Цельсия.
4 KIO3 = KI + 3 KIO4. H5IO6 – это кристаллическое вещество без цвета, температура плавления составляет 128 °C. Если нагреть H5IO6 до 100 °C в условиях вакуума, то образуется HIO4 (H5IO6 = HIO4 + 2H2O), которая при более высокой температуре разлагается, образуя 2 HIO3 и O2 (2HIO4 = 2HIO3 + O2). В водных растворах H5IO6 проявляет свойства слабой многоосновной кислоты.
Чтобы получить H5IO6, можно использовать обменную реакцию, например, Ba3(H2IO6)2 + 3H2SO4 = 2H5IO6 + 3BaSO4, с последующим выпариванием фильтрата. Периодаты – это кристаллические вещества, устойчивые к нагреванию и растворимые в воде. Эти вещества получаются электрохимическим окислением иодатов.
Растворение иода в воде — это сложный процесс, который включает растворение, диспропорционирование (I2 + H2О = HI + HIO) и разложение HIO (3 HIO = 2 HI + HIO3). Скорость диспропорционирования HIO очень высока, особенно в щелочных растворах (3 I2 + 6 NaOH = NaIO3 + 5NaI + 3H2O). Так как константа равновесия реакции I2 + H2О = HI + HIO низкая (K = 2×10 –13), иод присутствует в водном растворе в форме I2, а иодная вода, сохраненная в темноте, не разлагается и имеет нейтральную реакцию.
Одним из распространенных заблуждений является утверждение, что в состав зубной эмали входит галоген — хлор. Однако это не соответствует действительности, так как галогены, такие как фтор, являются важными компонентами для формирования зубной эмали.
Фтор играет ключевую роль в процессе минерализации эмали и защите зубов от кариеса. Его наличие помогает укреплять и улучшать структуру зубов, делая их более устойчивыми к кислотам и бактериям.
Поэтому, чтобы поддерживать здоровье зубов и эффективно бороться с зубными проблемами, важно правильно понимать состав зубной эмали и роль галогенов в этом процессе.
Фильтры обратного осмоса
Чтобы бороться с примесями и бактериями в воде, часто применяют фильтры обратного осмоса. В домашних условиях они устанавливаются под раковиной и могут задерживать до 98% примесей в воде.
Обратный осмос – способ разделения растворов на составляющие компоненты, при котором, молекулы воды через полупроницаемую мембрану, перемещаются из объема с меньшей концентрацией растворенных веществ в объем с более высокой концентрацией. Таким образом, фильтры обратного осмоса обеспечивают чистую воду, не содержащую примесей как в процессе обычного осмоса, а наоборот, сохраняют ее без примесей.
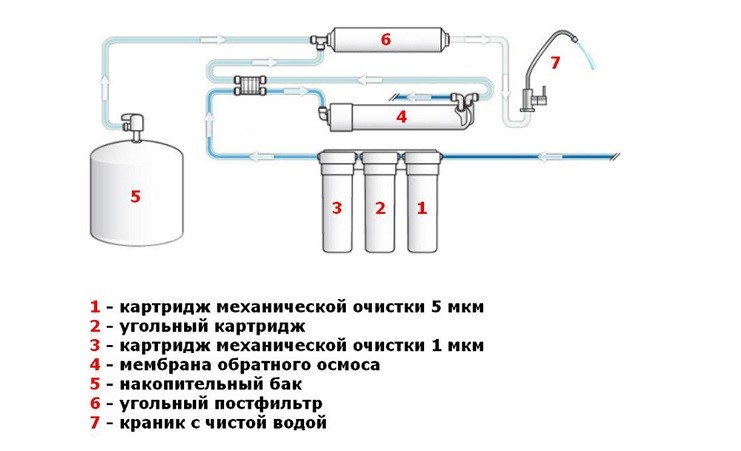
Система обратного осмоса является эффективным средством очистки воды от загрязнений.
При использовании данной технологии вода под высоким давлением пропускается через особую мембрану, которая способна пропускать только молекулы воды размером около 10⁻⁹ м, чем осуществляется ее очистка. Ионы хлора, железа и металлы пакетно смываются в дренаж вместе с грязью. Однако, в процессе очистки удаляются не только шлаки и микроорганизмы, но и минеральные вещества, которые необходимы для полноценного функционирования организма. По своим свойствам, очищенная вода становится схожей с «мёртвой» водой, лишенной минералов и солей.
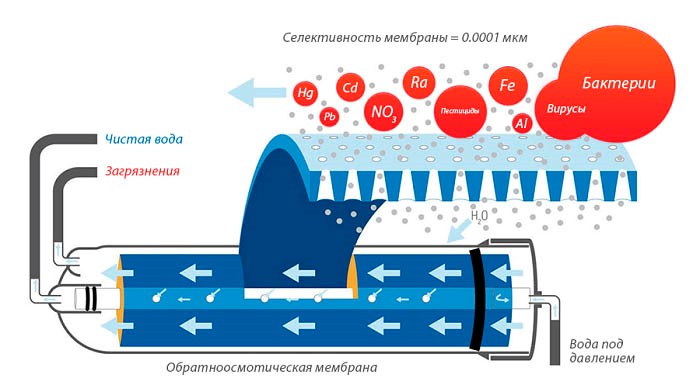
В регионах, где содержание фтора в воде превышает норму, необходимо использовать фильтры обратного осмоса для снижения риска развития флюороза. Однако, Верно и обратное утверждение: обратный осмос без фтора увеличивает вероятность развития кариеса из-за отсутствия фторапатита в составе эмаль. По этой причине этот метод очистки воды может быть рекомендован для взрослых, но не для детей, которым необходима надлежащая доза фтора. Например, можно использовать смешанный метод, чередуя очищенную воду с водой из крана.
В заключение
В прошлом принята практика отправлять детей из эндемических регионов в зоны с нормальным содержанием фтора в воде на каникулы, чтобы снизить вероятность развития флюороза. Такой подход давал свои плоды. В настоящее время этого не происходит, но есть надежда, что программа, направленная на нормализацию содержания фтора в питьевой воде в России, даст свои результаты в ближайшее время.
Либо нет, это может занять много времени. В любом случае, пока можно ознакомиться со статистикой распространения флюороза в России.
Не нужно беспокоиться, если вы взрослый человек, у вас крепкие здоровые зубы и вы планируете переехать в эндемичный регион. Ваша эмаль не будет поражаться, исключение составляют случаи, когда концентрация фтора в питьевой воде очень высокая.
Эта статья является исключительно образовательной, а не руководством к действию. Обязательно проконсультируйтесь со специалистом, прежде чем принимать какие-либо меры в отношении здоровья зубов.
- Блог компании Белая Радуга
- Новости науки и популяризация науки
- Здоровье и благополучие


