Перивентрикулярные очаги головного мозга представляют собой изменения в белом веществе, возникающие вокруг желудочков мозга. Их появление может быть связано с различными факторами, такими как гипоксия, сосудистые нарушения или инфекции. Эти очаги часто обнаруживаются при СТИ или МРТ и могут указывать на наличие неврологических заболеваний.
Симптоматика перивентрикулярных очагов может варьироваться в зависимости от их размера и размещения. У пациентов могут наблюдаться нарушения когнитивных функций, двигательные расстройства или судороги. Важно провести комплексное обследование для определения степени влияния этих изменений на здоровье и принять необходимые меры для лечения.
- Перивентрикулярные очаги головного мозга — это участки повреждения, расположенные вокруг боковых желудочков мозга.
- Симптомы могут варьироваться, но часто включают нарушения движений, когнитивные расстройства и проблемы с равновесием.
- У пациентов могут наблюдаться изменения в психическом состоянии, такие как депрессия или замедление мышления.
- Причины появления очагов могут быть связаны с сосудистыми заболеваниями, гипоксией или воспалительными процессами.
- Диагностика осуществляется с помощью МРТ, что позволяет выявить наличие и объем очагов.
- Лечение зависит от причин и может включать медикаментозную терапию и реабилитацию.
Результат МРТ — единичные перивентрикулярные очаги
Я прошла МРТ. Пожалуйста, помогите разобраться, насколько это опасно и что могут означать полученные результаты. Какое заболевание может быть связано с этими данными?
По итогам исследования, на снимках суб- и супратенториальных областей мозга выявлены единичные (в количестве трех) перивентрикулярные очаги: справа на уровне задних рогов боковых желудочков размером до 6х3 мм, слева до 5х3 мм и сверху правого бокового желудочка до 5 мм, без следов перифокального отека (они слабо гиперинтенсивные на Т2 FLAIR и Т2 ВИ, изоинтенсивные на Т1 ВИ и DWI). Других очаговых изменений в веществах больших полушарий, ствола, мозолистого тела и мозжечка не обнаружено.
Описание патологии
Согласно статистике, лейкоареоз головного мозга встречается у 5–9% новорожденных, причем среди них почти 80% — недоношенные дети. Данное заболевание связано с поражением белого вещества в перивентрикулярной области, находящейся рядом с желудочками мозга. Перивентрикулярная лейкопатия играет ключевую роль в развитии детского церебрального паралича.

Ключевую роль в патогенезе заболевания играет нарушение мозгового кровотока, на фоне которого нарушается питание самого мозга. Первыми страдают самые чувствительные отделы мозга — в перивентрикулярной области образуется отек белого вещества, который приводит к накоплению медиаторов воспаления и некротизации клеток мозга.
Перивентрикулярные очаги головного мозга представляют собой участки изменения мозговой ткани, расположенные рядом с желудочками мозга. Эти изменения могут возникать по различным причинам, включая гипоксию, воспалительные процессы и сосудистые заболевания. Как эксперт в этой области, я обращаю внимание на то, что данные очаги могут восприниматься как знак различных заболеваний и отклонений в работе центральной нервной системы, что требует внимательного анализа клинической картины.
Симптоматика, связанная с перивентрикулярными очагами, может варьироваться в зависимости от их расположения и степени повреждения тканей. В некоторых случаях пациенты могут испытывать головные боли, нарушения памяти или когнитивные расстройства. Также нередко наблюдаются проблемы с координацией движений, слабость в конечностях и различные неврологические симптомы, что может указывать на необходимость дополнительного обследования и диагностики.
Важно отметить, что наличие перивентрикулярных очагов не всегда означает наличие серьезного заболевания, однако их выявление требует комплексного подхода к лечению и наблюдению за состоянием пациента. Часто ряд современных методов исследования, таких как МРТ, позволяет более точно оценить степень изменений и определить дальнейшую тактику ведения пациента. В связи с этим, я рекомендую не игнорировать подобные находки и обращаться к специалистам для получения консультационной помощи.
Причины
- обвитие пуповины;
- преэклампсия и эклампсия;
- преждевременные роды;
- родовые травмы;
- проблемы внутриутробного развития;
- врожденные аномалии;
- синдром дыхательной недостаточности;
- продолжительная желтуха.
Дополнительные рисковые факторы включают заболевания матери, такие как сахарный диабет, хроническая анемия и нарушения функции щитовидной железы.
Пружинин Марк Юльевич, врач-педиатр
Наибольшая угроза лейкоареозом наблюдается у недоношенных детей. Чем ранее родился малыш, тем выше риски появления данного заболевания, что связано с нарушением адаптационных процессов в кровеносной системе недоношенных. Дети из группы риска должны проходить регулярные обследования и находиться под постоянным контролем для раннего выявления лейкомаляции.
Что происходит в мозге при лейкомаляции?
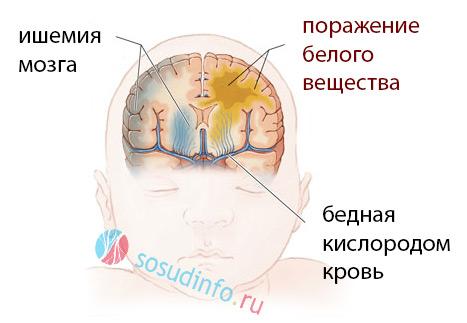
При лейкомаляции головного мозга в подкорковых структурах появляются очаги некроза, обычно – коагуляционного, гибнут нервные клетки, а дефекты замещаются размножающимися клетками микроглии наподобие того, как образуются рубцы в других органах. Нейроны не могут размножаться, и поля омертвения мозгу нечем заполнить, поэтому следствием их становятся кисты (полости) – кистозная лейкомаляция.
Более 50% случаев ПЛ сопровождаются вторичными геморрагиями в зоне ишемии и некроза, также могут происходить кровоизлияния в желудочки мозга. Примечательно, что поражение коры мозга у таких пациентов происходит крайне редко благодаря ее хорошему кровоснабжению.
Лейкомаляция обычно начинается в первые дни жизни и продолжается около недели после рождения. Возможно ее более позднее развитие, чаще всего из-за инфекции или дыхательной недостаточности новорожденного. В этих случаях на фоне уже существующих некрозов могут возникнуть новые очаги, что негативно сказывается на состоянии ребенка.
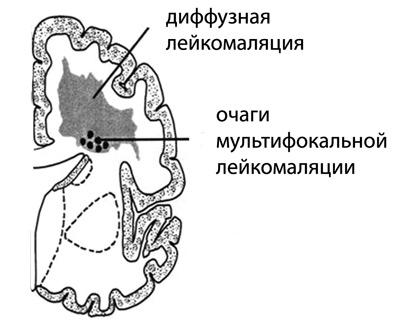
Очаги мультифокальной лейкомаляции диаметром 2-3 мм могут находиться в теменных и лобных долях, симметрично расположенные вокруг стенок боковых желудочков. В редких случаях затрагиваются височные и затылочные доли мозга. К последствиям некроза относится образование множества кист различного размера, распределенных по подкорковым слоям мозга (кистозная дегенерация), число которых со временем увеличивается. При тяжелой форме ПЛ они могут занимать всю перивентрикулярную область полушарий.
На некроз и образование кист уходит около двух недель, а последующие несколько месяцев в мозге малыша происходит спадение полостей, замещение погибших участков рубцами из нейроглии и необратимая атрофия нервной ткани.

лейкомаляции на снимках МРТ
Проявления лейкомаляции
Признаки лейкомаляции разнообразны и часто неспецифичны, но тяжелое гипоксическое повреждение мозговой ткани не может протекать бессимптомно. Выделяют несколько степеней ПЛ:
- Легкая степень – признаки повреждений нервной системы сохраняются в течение недели после рождения;
- Средняя тяжесть – от 7 до 10 дней, могут наблюдаться судороги, внутричерепная гипертензия и вегетативные нарушения;
- Тяжелая ПЛ – выраженное повреждение с угнетением функций головного мозга, нередко с переходом в кому.
Среди возможных проявлений церебральной лейкомаляции можно отметить:
- Повышенная нервно-рефлекторная возбудимость или, наоборот, снижение ее;
- Судорожные проявления;
- Гипотония мышц;
- Симптомы, связанные со стволом;
- Парезы и параличи;
- Проблемы со зрением, такие как косоглазие;
- Задержка психомоторного развития, нарушения интеллекта, гиперактивность и дефицит внимания.
Специалисты подчеркивают, что неврологическая симптоматика в остром периоде и до 3-5 месяцев жизни может быть минимально выраженной. Учитывается, что около 90% детей после острого периода показывают временное улучшение, которое может длиться до 5, иногда даже 8-9 месяцев. Лишь по истечении данного времени начинают проявляться симптомы дефицита неврологической активности на фоне атрофии мозговой ткани.
Вокруг желудочков мозга сконцентрированы проводящие нервные пути, ответственные за двигательную функцию конечностей, поэтому основным признаком церебральной лейкомаляции у детей становится детский церебральный паралич, но степень выраженности его зависит от массивности некроза.
Из-за затрагивания ствола мозга и черепных нервов большинство малышей страдает от косоглазия, часто сходящегося, а Возможны расстройства глотания и дыхательные проблемы. К шести месяцам жизни могут проявиться судороги. Чем больше площади некроза и число кист, тем более выраженной становится мозговая недостаточность. Симптоматика зависит от локализации патологий (двигательные и зрительные расстройства, судороги, задержки психического развития).
Серьезные поражения теменных и лобных долей могут вести к детскому церебральному параличу с сопутствующими нарушениями психического развития. Если задействованы только проводящие пути, отвечающие за иннервацию конечностей, паралич может протекать без нарушений интеллекта и развития ребенка.
У детей, перенесших перинатальную гипоксию, часто в числе симптомов могут оказаться дефицит внимания и гиперактивность при нормальном моторном развитии. Это относительно благоприятный вариант патологии, который поддается коррекции с помощью специальных лечебных мероприятий.
Ввиду такой непредсказуемости и разнообразия симптомов, маме бывает сложно разобраться, чего ожидать, когда малыш родился раньше срока и в условиях гипоксии. Если поражение носит умеренный или тяжелый характер, то ребенок не будет развиваться соответственно возрасту – не научится вовремя переворачиваться, сидеть и, тем более, ходить. Речевое развитие затормозится, малыш не сможет гулять, не будет следить за игрушками и проявлять такого характерного для своего возраста любопытства.
Гипертонус, который может вызывать болезненные ощущения, Вызывает беспокойство у детей, может приводить к плачу и нарушению сна. Проблемы с грудным вскармливанием могут возникать из-за недостаточного сосательного рефлекса, повышенной нервно-мышечной возбудимости или атонии.
Недостаточный прирост веса, замедленный рост, не соответствующий возрасту, и отсутствие умений, которые должен освоить растущий ребенок – это основные проблемы, с которыми сталкиваются родители детей с умеренной или легкой степенью повреждений подкорковых структур.
Примерно к году становится заметным неврологический дефицит, развивается церебральный паралич, задерживается психомоторное развитие. После года, когда восстановительный период подходит к концу, в клинике преобладают такие последствия, как задержка психоречевого развития, эмоциональная лабильность, проблемы со сном и вниманием, которые могут быть наряду с более тяжелыми моторными расстройствами (детский церебральный паралич).
Лейкомаляция у взрослых может приводить к церебральному параличу, гипертонусу, интеллектуальным нарушениям и тяжелой олигофрении. При благоприятном течении заболевания взрослые пациенты могут не отличаться от здоровых.
Основные причины возникновения лейкоареоза
Этиологические причины заболевания не выявлены. Основные факторы, способствующие его развитию:
- Инфекционные процессы с ишемией головного мозга;
- Неправильное питание;
- Возраст старше 50 лет;
- Малоподвижность;
- Повышенное внутричерепное давление;
- Болезнь Альцгеймера;
- Деменция;
- Гипертония;
- Ишемия, инсульт;
- Нарушение мозгового метаболизма.
Повышение артериального давления приводит к повреждению мелких артерий. Разрушение перивентрикулярных сосудов обеспечивает малую ишемию белого вещества.
Устойчивое повышение давления существенно увеличивает риск легкой ишемии. Наполнение артерий создает условия для увеличения их проницаемости.
Приблизительно у 40% больных причиной болезни становится недостаток cerebral blood supply. Болезнь Бинсвангера развивается из-за нехватки кислорода.
После 50 лет причиной могут быть аномалии сосудистой структуры, повреждение эндотелия, снижение эластичности артерий.
Метаболические нарушения в среднем возрасте с повышенным образованием гомоцистеина создают условия для повышения проницаемости артериальной стенки. Эндотелиальная дисфункция мелких капилляров создает предпосылки к развитию нозологии.
Основные клеточные элементы крови, отвечающие за восстановление поврежденных участков, это тромбоциты. Образование сгустков в мелких капиллярах может затруднять кровоток.
Нарушения дыхания во сне (апноэ) повышают риск сужения просвета бронхов. Храп может способствовать повышению артериального давления. Ослабление сосудистой стенки и потеря эластичности во время внутричерепной гипертензии увеличивает риск развития заболевания.
Прослеживается лейкоареоз у пациентов с сахарным диабетом первого или второго типа из-за развития метаболического синдрома, нарушения функциональности митохондрий. Недостаток поступления глюкозы в ткани головного мозга приводит к гипоксии, ишемии, патологии миркоциркуляции.
Степени лейкоареоза в молодом возрасте
Формирование патологических очагов и ишемических участков рядом с желудочками имеет различную степень выраженности.
Классификация лейкоареоза по морфологическим особенностям:
- 1 степень – незначительные проблемы с координацией, замедление ходьбы;
- 2 степень – наступление клинических признаков нарушений движений, ухудшение концентрации и памяти;
- 3 степень – заметное увеличение объема желудочков, усиление проявлений болезни. Такие пациенты нуждаются в наблюдении;
- 4 степень – неконтролируемое мочеиспускание, потеря равновесия, угнетение психомоторной активности.
Прогрессирование патологии занимает несколько лет. Морфологические изменения необратимы, поэтому лучше верифицировать мозговые нарушения первой степени, когда можно подобрать поддерживающее лечение.
Клинические симптомы у детей могут отсутствовать. Диагностика проводится, когда возникают трудности в лечении речевых нарушений.
Диагностика
При первых симптомах болезни диагностировать заболевание зачастую оказывается сложным, поскольку изменения могут быть незначительными и чаще всего единичными. Поэтому необходимы повторные обследования для установления изменений на снимках.
Типы исследований, назначаемых при подозрении на заболевание головного мозга:
- Компьютерная томография (КТ).
- Магнитно-резонансная томография (МРТ).
- Ангиография в сочетании с МРТ.
- Ультразвуковое исследование (УЗД) и допплерография.
- Рентгенография шейного отдела позвоночника.
- Электроэнцефалография (ЭЭГ).
- Регулярный мониторинг артериального давления (АД) (каждый день).

Обязательно проведение анализов на глюкозу, холестерин, проведение коагулограммы. При обнаружении сопутствующих патологий пациент направляется к узким специалистам. Кроме того, важно обнаружение истинной причины сосудистого генеза.
Методы терапии могут значительно различаться: хирургическим путем удаляются холестериновые отложения и тромбы, а также проводятся процедуры, направленные на нормализацию внутричерепного давления. Сильно пораженные сосуды могут быть удалены. Консервативная терапия предполагает разжижение крови, нормализацию кровообращения, устранение спазмов, снижение повышенного артериального давления, улучшение метаболических процессов, восстановление интеллектуальных функций и регенерацию поврежденных тканей. Устранение источника сосудистого генеза благоприятно сказывается на прогнозе. Однако игнорирование лечения может привести к инвалидности или летальному исходу.
Если наблюдаются неп pleasant симптомы, такие как головная боль и нарушения координации, необходимо выяснить их причины, а не просто снимать признаки. Постоянный контроль состояния здоровья и проведение профилактических осмотров имеют большое значение даже после постановки диагноза и лечения. Мы приглашаем всех посетить Чеховский сосудистый центр в Московской области, где предусмотрен широкий спектр диагностических возможностей для выявления заболеваний сердечно-сосудистой системы и консультации специалистов, которые знают о всех последних достижениях в области доказательной медицины. Мы индивидуально подбираем эффективные методы лечения, включая хирургические интервенции по строгим показаниям.
Что такое перивентрикулярные очаги головного мозга симптомы

Патологии
Клинический случай: 17-летняя девочка К. А. была госпитализирована в НИКИ Педиатрии имени Ю. Е. Вельтищева в марте 2018 года с фармакорезистентной эпилепсией. У неё наблюдались приступы, проявляющиеся внезапным и резким криком, психомоторным возбуждением и страхом на лице, иногда сопровождающиеся ороалиментарными автоматизмами (например, причмокиванием), продолжительностью 1-2 минуты, с частотой до 10 раз в месяц.
История жизни: Девочка родилась от первой беременности после досрочных родов на 36 неделе (с угрозой прерывания). При рождении её масса составила 2710 г, длина — 48 см, по шкале Апгар оценка составила 7/8 баллов. Сразу после рождения была обнаружена гемангиома слева на шее, которая имела тенденцию к росту (была проведена операция по склерозированию). Психомоторное развитие проходило в соответствии с возрастными нормами.
Наследственность по эпилепсии и психическим заболеваниям не отягощена.
История болезни: С 15 лет (2015 года) девочка начала жаловаться на состояния, которые сопровождались чувством страха, нехватки воздуха, звоном в ушах и ощущением, будто за спиной дышит собака. Ежедневно у неё появлялись цветные пятна перед глазами (по её словам, «цветные облачка синего и оранжевого цветов»).
Обследование на дому:
МРТ головного мозга (2015 год): патологии не обнаружено.
ЭЭГ (нативных данных нет): по описанию – эпилептиформная активность в лобно-височных областях, со склонностью к генерализации.
Была назначена ламиктал (2 мг/кг в день). Это привело к снижению частоты приступов до одного раза в неделю, однако при попытке увеличить дозу наблюдались побочные эффекты в виде аллергической сыпи.
С декабря 2016 года приступы изменились — они начинались с внезапного крика с мольбой о помощи, с ярко выраженным психомоторным возбуждением, страхом на лице и ороалиментарными автоматизмами в конце.
На контрольной ВЭЭГМ с записью сна: типичной эпилептиформной активности не выявлено. В связи с подозрением на неэпилептический генез приступов, выставлен предварительный диагноз: Панические атаки, с отменой ламиктала. Приступы стали ежедневными. Повторное введение ламиктала без результата.
К терапии была добавлена вальпроевая кислота, а позже — финлепсин, который плохо переносился (тошнота, рвота, сыпь) и не дал терапевтического эффекта. При дальнейшем подборе лечебной схемы (Кеппра + Вимпат + Ламиктал в начальных терапевтических дозах) удалось добиться уменьшения частоты приступов. Однако полной ремиссии достичь не удалось.
На момент госпитализации девушка принимала комбинированное лечение: Кеппра 10 мг/кг/день, Вимпат 6 мг/кг/день и Ламотриджин.
В стационаре отмечалось 2 приступа с внезапным криком, чувством страха, психомоторным возбуждением (бежит к окну, пытается открыть его).
Осмотр: Масса тела 50 кг, рост 158 см. Уровень интеллекта соответствует возрасту, учится в колледже, успеваемость хорошая. Очаговой симптоматики нет. Никаких нарушений координации не выявлено.
В связи с отсутствием эпилептиформной активности на представленном ВЭЭГМ (2016 г.), нормальной МРТ и особенностями хроники приступов был проведен дифференциальный диагноз между психогенными неэпилептическими приступами, паническими атаками и эпилепсией. Выполнен видео-ЭЭГ-мониторинг на 2-й и 7-й день после отмены антиэпилептических препаратов.
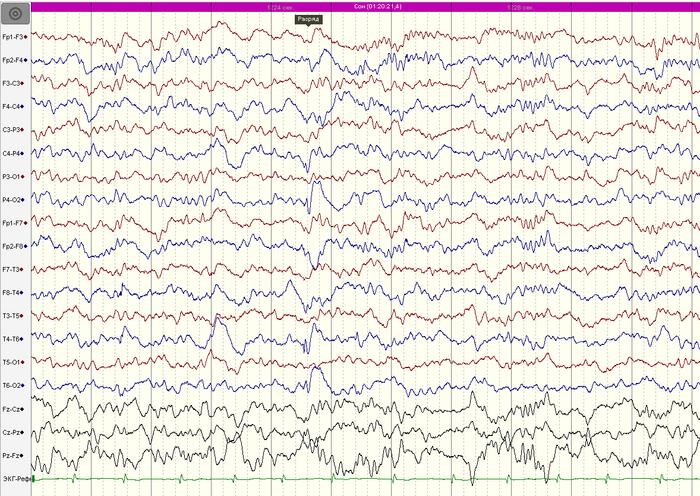
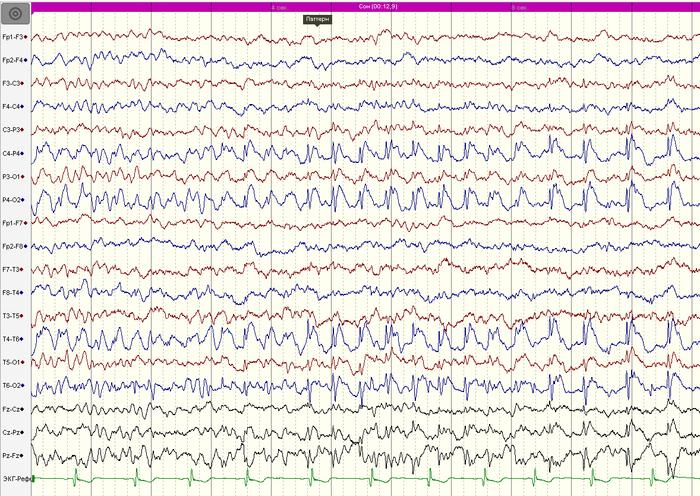
ВЭЭГ-мониторинг (на 2-й день отмены АЭП): основной ритм и физиологические образцы сна формированы соответствующе возрасту. Обнаружена эпилептиформная активность в правой задневисочно-теменно-затылочной области (Т6-Р4-О2) с низким индексом (рис.1).
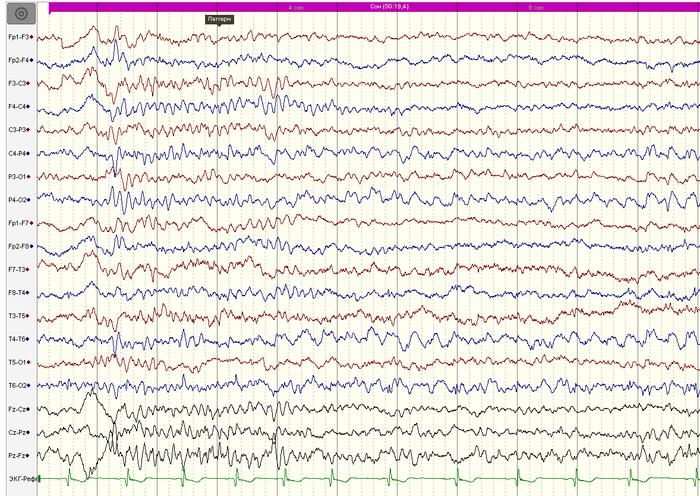
ВЭЭГ-мониторинг (на 7 день отмены АЭП): региональная эпилептиформная активность в правой задневисочно-теменно- затылочной области ( T6-P4-02) . Однократно во сне зарегистрирован субклинический иктальный паттерн в правой задневисочно-теменно-затылочной области, длительностью до 20 секунд (рис.2-3).
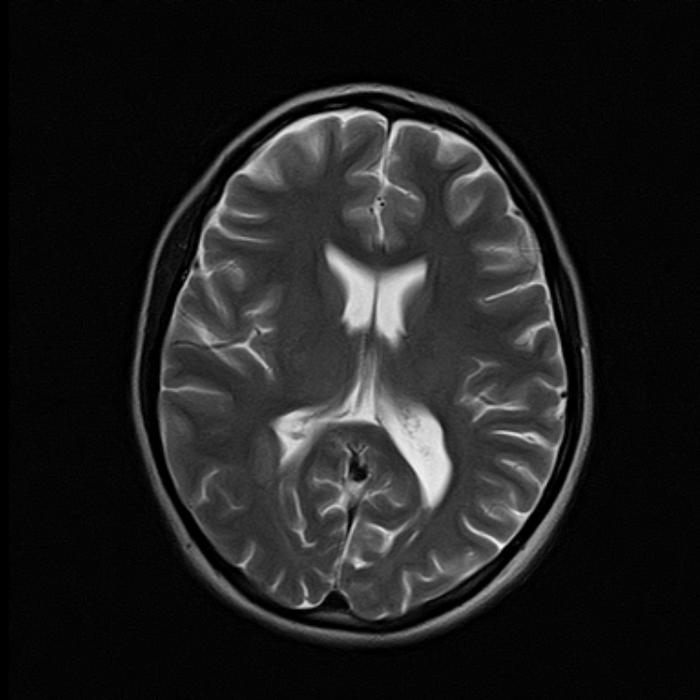
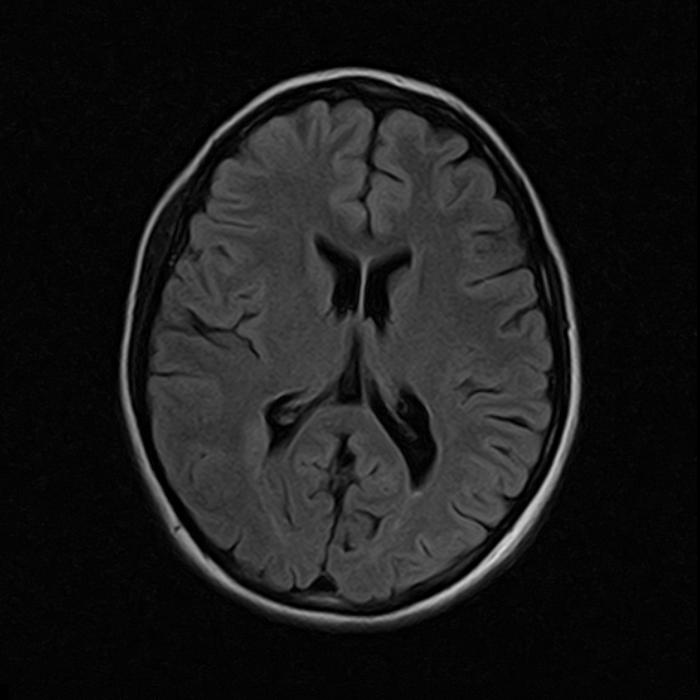
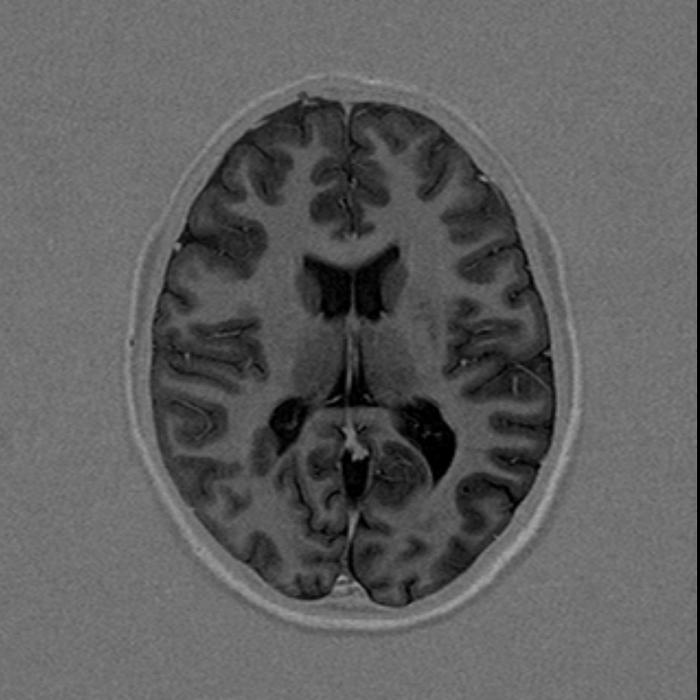
В проекции заднего рога правого бокового желудочка обнаружен участок гетеротопии серого вещества размером 18х12 мм, который поджимает задний рог бокового желудочка. Заключение: МРТ-картина узловой гетеротопии в области правого бокового желудочка.
МРТ головного мозга (март 2018):
С учетом клинико-ЭЭГ данных и результата магнитно-резонансного исследования мозга установлен диагноз: Порок развития головного мозга (узловая гетеротопия). Структурная фокальная эпилепсия. Фармакорезистентность.
Также была скорректирована противоэпилептическая терапия, рекомендована монотерапия препаратом Вимпат с медленным увеличением дозы, при хорошей переносимости, до 8 мг/кг/день.
Запланировано предхирургическое обследование для принятия решения о хирургическом вмешательстве.
Пациент информирован о возможности проведения молекулярно-генетическое обследования с целью генетического подтверждения диагноза.
Резюме: представлен случай подростка с нормальным уровнем интеллектуального развития, который жалуется на кратковременные дневные приступы, сопровождающиеся страхом и психомоторным возбуждением, сильно напоминающие психогенные неэпилептические расстройства и панические атаки. В результате проведения ВЭЭГ мониторинга после отмены противоэпилептической терапии была выявлена четкая эпилептиформная активность, соответствующая зоне аномалии головного мозга.
Таким образом, в некоторых случаях у пациентов с фармакорезистентными приступами неопределенной этиологии, при отсутствии эпилептиформной активности на ЭЭГ, может быть применена полная отмена антиэпилептических препаратов в стационаре перед видео-мониторингом.
Перивентрикулярная нодулярная (узловая) гетеротопия (РNH) – это аномалия развития головного мозга, возникающая на фоне нарушения миграции нейронов и проявляющаяся образованием узлов серого вещества вдоль боковых желудочков. Данное нарушение происходит на раннем этапе развития плода между 6 и 24 неделями беременности.
В зависимости от расположения узлов перевентрикулярная гетеротопия может быть: 1)билатеральная и симметричная, 2)билатеральная с единичными узлами, 3)билатеральная/асимметричная,4)унилатеральная, 5)унилатеральная с распространением в кору (Battaglia G.,Chiapparini L.2006). Генетические факторы играют более важную роль в развитии билатеральной гетеротопии в отличие от унилатеральной.
Билатеральная нодулярная гетеротопия часто связана с мутациями в гене FLN (Xq28). Обычно мальчики погибают, а в редких случаях рождаются с тяжелыми аномалиями мозга, в то время как у девочек мутации приводят к образованию нодулярной гетеротопии. Редко встречается мутация в гене ARFGEF2 (V. Passarelli et al. 2014, M.Chen, C.Walsh, 2002).
Гетеротопия может быть как изолированной (простая форма), так и сочетаться с другими аномалиями мозга (PNH plus).
По результатам исследования (d’Orsi G. и Tinuper P. et al. 2003) описаны различия в клинических проявлений и исходах в зависимости от формы перивентрикулярной гетеротопии. Для пациентов с простыми формами нодулярной гетеротопии было характерно нормальное интеллектуальное развитие, иногда в сочетании с дислексией (Marcia V. Felker, M.D.et al.2011).
Первое появление приступов (чаще всего фокальных) обычно наблюдается в подростковом возрасте с благоприятным течением на фоне приема противоэпилептических препаратов (исчезновение или уменьшение частоты приступов). На ЭЭГ, несмотря на нормальный основной ритм, фиксируются фокальные изменения (эпилептиформные разряды или неспецифическая тета-активность). У пациентов с нодулярными гетеротопиями, сопутствующими другим аномалиям мозга (PNH plus), наблюдаются отклонения в раннем психомоторном развитии, а также развитие когнитивных дефицитов различной степени тяжести, расстройства поведения и неврологические дефициты, например, гемипарез. Эпилептические приступы часто начинаются в первые 10 лет жизни. Как правило, у таких пациентов отмечаются высокая частота как фокальных, так и генерализованных приступов с рефрактерным течением.
Многие исследователи приводят примеры успешного хирургического лечения после резекции изолированных периферических нодулярных гетеротопий (Sherer C, Schuele S., et al. 2005; Schmitt FC, Voges J 2011).
В 2012г. Takashi A и соавтор. описали случай успешного хирургического лечения пациента с фармакорезистентной эпилепсией, обусловленной единичной нодулярной гетеротопией. Было проведена резекция перивентрикулярного узла, несмотря на то, что прехирургическое обследование данного пациента, в том числе инвазивное стерео-ЭЭГ, показало несоответствие зоны начала приступа расположению гетеротопиона. По мнению исследователей это обусловлено сложным механизмом эпилептогенеза с образованием нейрональных сетей между гетеротопионом и окружающим кортексом.
Лечение глиоза
Поскольку замещение нейронов глиозными очагами является необратимым процессом, то данное патологическое состояние не поддается лечению. Основное направление терапии — это лечение основного заболевания, которое вызывает эту патологию (гипертоническая болезнь, сахарный диабет, атеросклероз, посттравматические осложнения и так далее).
В то же время, при выраженной нейро-симптоматике, рекомендуется назначать медикаменты (индивидуально в зависимости от симптомов), направленные на улучшение проводимости нервных волокон, укрепление стенок кровеносных сосудов и повышение их эластичности, улучшение активности мозга и когнитивных функций.
Рекомендуются препараты, способствующие уменьшению агрегации тромбоцитов и укреплению сосудистых стенок: Аскорутин, Тромбо АСС, Плавикс, Тиклид, Курантил, а Витаминные комплексы.
Для снижения темпов прогрессирования атеросклероза могут назначаться гиполипидемические средства — фибраты/статины: Аторвастатин, Ловастатин, Розувастатин, Фенофибрат.
Для нормализации кратковременной памяти, физической ориентации и устранения поведенческих нарушений может быть выписан экстракт листьев Гинкго Билоба или Танакан.
Для улучшения внимания и памяти пациентам с когнитивными расстройствами, основной причиной которых являются сосудистые проблемы мозга, рекомендуется вводить в больших дозах такие препараты, как Церебролизин и Кортексин.
При нейроинфекциях назначаются антибактериальные препараты/противовирусные препараты в зависимости от патогена, вызвавшего нейроинфекцию. При выраженных головных болях — анальгетики: Кетанов, Анальгин и др.
Пациенты обязаны регулярно следить за своим весом и артериальным давлением, придерживаться низкокалорийной, богатой витаминами диеты, заниматься оздоровительной гимнастикой, а также поддерживать как физическую, так и умственную активность. Это может включать чтение, запоминание стихов, просмотр телепередач, общение с родными и близкими, прослушивание музыки, изучение иностранных языков и другие активности.
Лечение перивентрикулярного лейкоареоза головного мозга
Вопрос о том, как лечить лейкоареоз головного мозга, решается врачом на основе комплексного обследования и определения этиологии заболевания.
Специфическая терапия, направлена на возобновление прежней структуры белого вещества мозга отсутствует.
Главная терапия сосредоточена на замедлении прогрессирования патологических процессов, снижении выраженности симптомов и восстановлении мозгового кровообращения.
Эффективно применяются медикаментозные препараты, которые способствуют улучшению обменных процессов, нормализации кровообращения и снятию мышечного напряжения.
Также проводится лечение основной болезни, которая послужила причиной для появления патологических изменений.

МРТ для диагностики перивентрикулярного лейкоареоза головного мозга
При наличии депрессивных состояний могут быть применены успокаивающие и психотропные медикаменты.
Назначаются лечебные упражнения и массаж, которые помогают восстановить двигательную активность.
Первоначально упражнения подбираются квалифицированным специалистом, программа разрабатывается в зависимости от тяжести состояния больного и его функциональных возможностей. При возможности рекомендуется посещать бассейн, совершать пешие прогулки на свежем воздухе.
Если болезнь не будет вовремя диагностирована, то будет крайне сложно замедлить её прогресс, что чревато развитием ишемического инсульта.
Медикаменты
Медикаментозная терапия включает в себя:
- ноотропные медикаменты (препараты, которые положительно влияют на умственные функции, улучшают кровообращение в мелких сосудах, повышают память, устойчивость мозговых структур к различным неблагоприятным воздействиям,
предотвращают образование тромбов и улучшают метаболизм в клетках мозга) – из наиболее популярных можно выделить Пирацетам, Эуфиллин, Нитроглицерин; - лекарства для снижения артериального давления – диуретики, бета-адреноблокаторы, ИАПФ;
- витамины группы В, которые способствуют улучшению клеточного метаболизма;
- препараты для улучшения мозгового кровообращения – Актовегин, Циннаризин.
Народные методы
Помимо традиционной терапии широко применяются различные методики народного лечение.
Использование фитотерапии может усилить действие медикаментов и помочь улучшить кровоток.

Отвар корней валерианы для лечения перивентрикулярного лейкоареоза мозга
Рецепты народной медицины помогают справиться с депрессией, снижают уровень раздражительности и в целом оказывают положительное влияние на психоэмоциональное состояние пациента.
Применяются лекарственные отвары после консультации с врачом:
- Для приготовления отвара из корней валерианы требуется 15 г растения, которые заливают 250 мл кипятка, доводят до кипения и выдерживают на огне 20-30 минут, затем снимают с плиты, накрывают крышкой и оставляют настаиваться еще на 40 минут; процедив отвар, принимают по 1 ст. ложке до 4 раз в день;
- Три столовые ложки соцветий боярышника заливаются 600 мл кипящей воды, накрываются и настаиваются в темном месте около 1-2 часов; принимают по 1/3 стакана дважды в день за 40 минут до еды;
- Для настоя из цветков ромашки 4 столовые ложки растения заливаются 200 мл кипящей воды и настаиваются несколько часов; рекомендуемая дозировка – по 125 г утром после еды.
Прогноз на жизнь
Это заболевание склонно к быстрому развитию, однако раннее обнаружение и лечение позволяют существенно замедлить его прогрессирование, улучшить самочувствие пациента и избежать серьезных нарушений в работе центральной нервной системы.
Тем не менее, даже несмотря на замедление прогрессирования, со временем состояние может ухудшаться, что приводит к разрушению мозговой структуры.
В результате заболевание приводит к стойкому расстройству психического здоровья, слабоумию.
Перивентрикулярный лейкоареоз представляет собой одну из редких и тяжелых патологий головного мозга, возникающую в результате нарушений нормального кровообращения, при этом специфического лечения для данной болезни не существует.
Сохранить как можно дольше интеллектуальные, мыслительные и двигательные функции возможно исключительно при условии ранней диагностики, адекватной медикаментозной терапии и отказа от вредных привычек.
Опыт других людей
Анна, 32 года, врач: «Когда мне поставили диагноз, я была в шоке. Врач объяснил, что перивентрикулярные очаги могут указывать на различные заболевания, включая рассеянный склероз. Я стала замечать, что у меня начали появляться головные боли и иногда возникали проблемы с координацией движений. Научилась прислушиваться к своему телу и теперь регулярно прохожу обследования.»
Сергей, 45 лет, инженер: «Я узнал о перивентрикулярных очагах, когда проходил МРТ из-за сильных головокружений. Ошеломление было сильным, когда я услышал о возможных симптомах — от слабости до проблем с речью. У меня начали появляться небольшие провалы в памяти. Врач посоветовал мне обратить внимание на питание и стресс, и я решил изменить свой образ жизни.»
Елена, 28 лет, студентка: «Мы с группой делали проект по неврологии, и я наткнулась на информацию о перивентрикулярных очагах. Это меня заинтриговало, и я начала изучать симптомы. Узнала, что они могут проявляться в форме изменений настроения, усталости и проблем с концентрацией. На личном уровне, я всегда старалась следить за своим состоянием, после ярких примеров из учебных исследований, я поняла, как важно обращать внимание на здоровье.»
Вопросы по теме
Как перивентрикулярные очаги могут повлиять на когнитивные функции?
Перивентрикулярные очаги могут негативно сказываться на когнитивных функциях, так как они расположены вблизи важных структур головного мозга, отвечающих за память, внимание и исполнительные функции. Поражение этих областей может вызывать трудности с концентрацией, снижением памяти и даже изменение личности. Симптомы могут варьироваться от легкого замедления мышления до более серьезных нарушений, таких как деменция.
Как врач может диагностировать перивентрикулярные очаги?
Врач может использовать различные методы диагностики для выявления перивентрикулярных очагов. Наиболее распространенным методом является магнитно-резонансная томография (МРТ), которая позволяет получить четкие изображения головного мозга и выявить даже небольшие изменения в его структуре. Иногда могут быть назначены дополнительные исследования, такие как компьютерная томография (КТ) или исследование цереброспинальной жидкости.
Какие факторы могут способствовать образованию перивентрикулярных очагов?
Существует несколько факторов, способствующих образованию перивентрикулярных очагов. К ним относятся гипертония, диабет, атеросклероз и другие сосудистые заболевания. Также повышенный риск связан с возрастом и нарушениями кровообращения, такими как инсульт. В некоторых случаях такие изменения могут быть ассоциированы с хроническими воспалительными процессами или инфекциями.




